甲、乙、丙三种物质的溶解度曲线,如图所示,回答下列问题:
(1)P点的含义 ;
(2)t 2℃时,甲、乙、丙三种物质溶解度从大到小的顺序为 ;
(3)当乙中混有少量甲时,可采用 (填"降温结晶"或"蒸发结晶")的方法提纯乙。
(4)t 2℃时,将甲、乙、丙三种物质的饱和溶液同时降温t 1℃,所得溶液中溶质质量分数由大到小的顺序为 。

用赤铁矿(主要成分Fe2O3)为原料,炼铁的主要反应的化学方程式是____________________________________.在这一反应中,铁元素的化合价由____________价变为____________价。
实验室用浓盐酸(溶质质量分数为37%,密度为1.18g·mL-1)配制100g溶质质量分数为10%的稀盐酸。
(1)计算:需要浓盐酸mL,水mL。(结果保留小数点后一位)
(2)量取:用规格为mL的量筒(从50mL、100 mL中选择)量取浓盐酸,倒入烧杯中,再用规格为mL的量筒(从50mL、100 mL中选择)量取水。
(3)稀释:_。
向装有等量水的A、B、C烧杯中分别加入10g、25g、25gNaNO3固体,充分溶解后,现象如图一所示。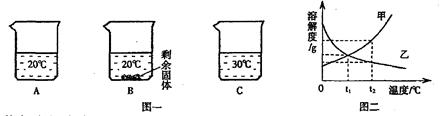
(1)烧杯中的溶液一定属于饱和溶液的是(填序号);
(2)图二能表示NaNO3溶解度曲线的是(填“甲”或“乙”);
(3)欲除去混在甲中的少量乙物质将可采用的方法是;
(4)由图二分析,若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的(填序号)。
A.甲、乙都是饱和溶液B.所含溶剂质量:甲<乙
C.溶液质量:甲>乙D.溶质质量分数:甲>乙
完成下列变化的化学方程式,并按要求填空。
(1)常温下,金属铝和氧气反应,在铝表面生成;该反应表示为。
(2)将氯化氢和氨气两种无色气体混合,生成氯化铵固体:;反应类型为。
(3)氢氧化钠溶液中滴加硫酸铜溶液反应:;反应现象为。
(4)实验室用一氧化碳还原三氧化二铁:;硬质粗玻璃管中的现象为。检验上述反应的气体产物的化学方程式:;检验上述反应的固体产物,除了观察外观、用磁铁吸引以外,还可用化学方法,化学方程式为:,此反应(填 “放出”或“吸收”)热量。尾气可用法来处理。
试选用“>”或“<”或“=”填空。
(1)空气中气体成分的体积分数:氧气稀有气体;
(2)通常状况下的液体体积:100mL酒精与100mL水混合200mL。
(3)室温下,1g硝酸钾饱和溶液中加入1g硝酸钾固体能得到溶液的质量2g
(4)相同的两段细铁丝生锈的速率:用蒸馏水浸过的铁丝用食盐水浸过的铁丝
(5)1g硫粉在1g氧气中完全燃烧后生成二氧化硫的质量2g
(6)熔点:武德合金其组成金属