某校学校小组的同学为了测定某石灰石中碳酸钙的质量分数,他们取该石灰石样品10g加入烧杯中,再把80g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的杂质既不溶于水,也不与稀盐酸反应):
实验次数 |
第1次 |
第2次 |
第3次 |
第4次 |
加入稀盐酸的质量/g |
20 |
20 |
20 |
20 |
剩余固体的质量/g |
7 |
4 |
2.6 |
m |
分析表中数据,完成下列问题:
(1)表中m的数值为 ;
(2)该石灰石样品中碳酸钙的质量分数为 ;
(3)计算第一次试验反应结束后所得溶液中溶质质量分数(计算结果精确到0.1%)
若使100g溶质质量分数为10%的氯化钠溶液变成20%的氯化钠溶液,
⑴下列可以达到目的的方法是(选填序号)。
| A.加水 | B.加溶质 | C.蒸发溶剂 | D.倒出一些原溶液 E.倒入一些原溶液 |
F.加入一定量5%的氯化钠溶液 G.加入一定量25%的氯化钠溶液
⑵请在你选的方法中选择一项,计算出加入或减少物质的质量(写出计算过程)。
计算过程:
乳酸(C3H6Ox)是一种重要的体内代谢物。其相对分子质量为90。求:
⑴x的值为;
⑵每个乳酸分子中碳、氢原子个数比为;
⑶180g乳酸中含碳元素为g。
小强在家庭装修的废弃料中看到一些大理石碎料,他想探究大理石中碳酸钙的含量。于是他取部分大理石带到实验室,砸碎后称取25g,加入200g稀盐酸恰好完全反应,测得生成二氧化碳的质量为8.8g。
求:⑴大理石中碳酸钙的质量分数。
⑵所用稀盐酸的溶质质量分数。
微型化学实验使用药品的量很少,产生的废弃物也很少,因此被誉为绿色环保的化学实验。用如图微型仪器完成制取并检验CO2的实验只消耗了0.55 g 10%的盐酸。求:(1)产生CO2的质量是多少克?(结果保留三位小数)(2)如果10%的盐酸密度为1.1g/cm3,消耗盐酸的体积是多少毫升?(3)通常完成这个实验大约需10%的盐酸5 mL,这是微型实验用药量的多少倍?
实验室有一瓶未知浓度的BaCl2溶液,某同学取出150g该溶液于烧杯中,向其中逐滴加 入溶质质量分数为26.5%的Na2CO3溶液。反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图甲所示。已知:BaCl2+Na2CO3=BaCO3↓+2NaCl
入溶质质量分数为26.5%的Na2CO3溶液。反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图甲所示。已知:BaCl2+Na2CO3=BaCO3↓+2NaCl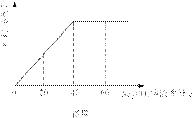
请计算:(1)配制26.5%的Na2CO3溶液80g,需要Na2CO3固体多少 g。
(2)BaCl2溶液的溶质质量分数是多少?(写出计算过程,结果保留到0.1%)