元素周期表中,某周期元素的原子结构示意图如下:
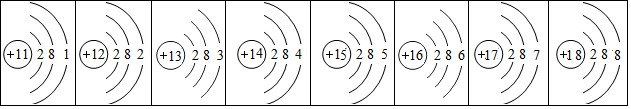
根据以上信息,回答下列问题:
(1)该周期有 种金属元素。
(2)该周期的元素从左至右,其原子核外电子排布的变化规律是 。
氢能是人们积极利用的新能源。根据下列装置回答:

(1)用A装置进行电解水实验,在甲试管内收集到的气体是 。
(2)实验室制取氢气,可用以下药品中的 (填序号)。
①银和稀盐酸②锌和稀硫酸③氧化锌和稀盐酸
(3)B装置是氢氧燃料电池,它把氢气和氧气反应的 能直接转化为电能。这类电池已在宇宙飞船、太空站等航天器上使用,发电后的产物为 ,还可供宇航员饮用。
(4)研究人员最新研发出CO2经过“烟囱”变燃料的技术:让CO2和H2混合后通过有镍纳米粒子的细铝管道,加热,在管道另一端出来的就是燃料。反应原理为:CO2+4H2 X+2H2O,其中X的化学式为 ,镍纳米粒子在反应中起 作用。
X+2H2O,其中X的化学式为 ,镍纳米粒子在反应中起 作用。
中国本土科学家屠呦呦获得2015年诺贝尔生理学或医学奖,她的突出贡献是创制新型抗疟药﹣﹣青蒿素和双氢青蒿素,挽救了全球特别是发展中国家的数百万人 的生命。回答:
(1)青蒿素的化学式为C15H22O5,它属于 (填“无机物”或“有机物”)。
(2)利用乙醚提取青蒿素的主要流程是:干燥、破碎青蒿叶→在乙醚中浸泡、萃取→浓缩提取液→粗品→精制。其中“破碎青蒿叶”主要发生了 变化。
(3)医生用青蒿素给病人治疗的同时,让其多吃蔬菜,目的是补充病人体内所需营养素中的 。
(4)青蒿中不仅含有青蒿素,还含有青蒿甲素(C15H22O3),它与青蒿素的组成元素 (填“相同”或“不同”)。
用化学用语填空:
(1)氮元素 ;
(2)两个钾离子 ;
(3)氧化钙 ;
(4)人体胃酸的主要成分 ;
(5)氢氧化铜 ;
(6)硫酸亚铁 。
填写实验报告.
|
实验内容 |
实验现象 |
分析、结论及解释 |
|
(1)测定碱溶液的pH 取两片pH试纸,放在白瓷板上,分别用玻璃棒蘸取稀氢氧化钠溶液,将试纸显示的颜色与 比较,读出pH. |
/ |
若实验过程中,用沾有水的玻璃棒蘸取溶液,则所测得的pH (填“>”、“=”或“<”)实际值 |
|
(2)碱和指示剂作用取两只洁净的试管,分别加入约2mL的稀氢氧化钠溶液,澄清石灰水,再分别加入3滴无色酚酞溶液,观察溶液颜色变化. |
两只试管汇中的酚酞溶液均变为 色 |
稀氢氧化钠溶液、澄清石灰水都呈 性. |
|
(3)碱和非金属氧化物的反应用排水法收集一瓶呼出的气体,然后加入约2mL澄清石灰水,振荡,观察现象 |
澄清石灰水变浑浊 |
反应的化学方程式
|
原子序数为1﹣18的元素的原子结构示意图等信息如图,请认真回答下列问题。

(1)原子序数为12的元素位于元素周期表中第 周期,它属于 (填“金属”或“非金属”)元素。
(2)在化学反应中,原子序数为16的元素的原子容易 (填“得到”或“失去”)电子,所形成的粒子的符号是 。
(3)根据氟原子和氯原子的结构示意图分析,由于氟原子和氯原子的 相同,所以氟元素与氯元素的化学性质相似。
(4)同周期元素,从左到右,各元素原子随原子序数的增加,最外层电子数依次 。