某热水壶中水垢的成分是Mg(OH)2和CaCO3,某同学通过实验测定水垢中CaCO3的量:向20.8g该水垢中逐滴缓慢加入稀盐酸,将产生的气体通入足量NaOH溶液中,当加入182.5g稀盐酸时,水垢恰好完全反应,此时NaOH溶液的质量增加6.6g。(不考虑盐酸挥发)
(1)CO2与足量NaOH溶液反应的反应方程式 。
(2)水垢与稀盐酸反应生成CO2的质量是 g。
(3)水垢中CaCO3的质量是 g。
(4)计算稀盐酸的溶质质量分数。(写出计算过程)
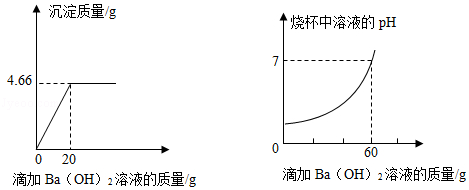
某混合溶液中含有硫酸和盐酸,取该混合溶液20g于烧杯中,不断滴加氢氧化钡溶液,反应过程中烧杯中产生沉淀的质量、溶液pH的变化如图所示(BaCl 2溶液呈中性)。求:
(1)完全反应后生成沉淀的质量为 g;
(2)计算20g混合溶液中HCl的质量为多少?
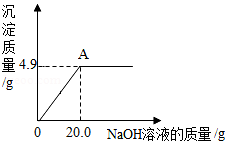
为了测定某硫酸铜溶液的质量分数,小杨同学取50.0g样品置于烧杯中,逐滴加入氢氧化钠溶液,加入氢氧化钠溶液质量和生成沉淀质量的关系如图所示。请计算:
(1)NaOH的化学式量为 。
(2)硫酸铜刚好完全反应时,所得溶液的质量为 g(保留一位小数)。
(3)硫酸铜溶液中溶质的质量分数是多少?(写出计算过程)
有一袋已部分变质的Ca(OH) 2(含杂质CaCO 3)固体样品,把该样品投入足量水中,充分搅拌后通入二氧化碳,沉淀质量与反应的二氧化碳质量关系如图所示。【提示:CO2+Ca(OH)2=CaCO3↓+H2OCO2+CaCO3+H2O=Ca(HCO3)2】
请回答下列问题
(1)Ca(OH) 2由 元素组成,其中H元素与O元素的原子个数比为 ;
(2)碳酸钙(CaCO 3)的相对分子质量为 ;
(3)生成沉淀最多时,参加反应的气体质量为 g;
(4)计算样品中碳酸钙的质量分数。(要求写出计算过程,结果精确到0.1%)

某纯碱样品中含有少量的氯化钠。取该样品13.9g完全溶于206.1g水中,加入90g CaCl 2溶液,恰好完全反应
后生成沉淀的质量为10g。求:
(1)生成的沉淀物的化学式为: ;
(2)样品中碳酸钠的质量为: g;
(3)反应后溶液中溶质质量分数。(要求写出计算过程)
食用小苏打含有 NaHCO 3外还含有少量NaCl.为了测定某食用小苏打中NaHCO 3的质量分数,某同学做了如下实验:称取一定量该样品于烧杯中,加水使其完全溶解,得到104.4g溶液,再向其中滴加100g稀盐酸,恰好完全反应时得到200g溶质质量分数3.1%的不饱和溶液。(反应的化学方程式为:NaHCO 3+HCl═NaCl+H 2O+CO 2↑)请计算:
(1)NaHCO 3中碳、氧元素的质量比为 ,
(2)生成CO 2的质量为 g,
(3)该食用小苏打中 NaHCO 3的质量分数(写出计算过程)。