小华有一只银手镯(银锌合金),她想用实验探究手镯中银的含量。先用电子秤称得手镯的质量是25.00克,再用稀盐酸分多次与此手镯充分反应。实验数据如下表:
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
|
加入稀盐酸的质量(克) |
10.00 |
10.00 |
10.00 |
10.00 |
10.00 |
充分反应后剩余固体的质量(克) |
24.35 |
23.70 |
23.05 |
23.00 |
23.00 |
根据上表中数据分析,完成下列问题:
(1)手镯中银的质量是 克。
(2)所用稀盐酸中溶质的质量分数是多少?
现有硫酸和硫酸铜的混合溶液200g,向该溶液中滴加入溶质质量分数为10%的氢氧化钠溶液直至生成氢氧化铜沉淀,生成沉淀的质量与加入氢氧化钠溶液的质量之间的关系如图,求: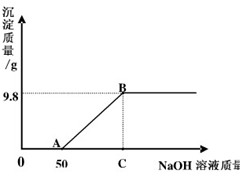
(1)氧化铜的相对分子质量;
⑵生成沉淀最多时所加入的氢氧化钠溶液的总质量。
有一瓶标签破损的稀硫酸(如右图1),为测定其溶质质量分数,取出7 g该溶液,加入足量的锌粒,产生氢气的质量与反应时间关系如右图2。请计算:该溶液中溶质的质量分数。
(化学方程式:Zn + H2SO4 ="=" ZnSO4 +H2↑)
过氧乙酸是一种高效广谱杀菌剂。水灾过后,为预防灾区发生瘟疫,常用0.2%的过氧乙酸溶液进行环境的表面消毒。对于20%的过氧乙酸溶液8Kg,请计算:
(1)含溶质过氧乙酸多少千克?
(2)可稀释成0.2%的过氧乙酸溶液多少千克?
汽车尾气系统中使用催化转化器,可降低CO、NO等有毒气体的排放,减少空气污染,其反应的化学方程式为2CO + 2NO  2CO2 + N2。当有11.2 g CO被转化时,计算同时被转化的NO的质量。
2CO2 + N2。当有11.2 g CO被转化时,计算同时被转化的NO的质量。
过氧乙酸是一种常用的消毒剂。请计算:
(1)要配制100 g溶质质量分数为15%的过氧乙酸溶液,需要过氧乙酸g;
(2)向100 g该溶液中加入200 g水,则所得稀溶液的溶质质量分数为。