二氧化锰因在工业生产中应用广泛而备受关注,制备二氧化锰是一项有意义的工作,某研究性小组对此展开了系列研究。
Ⅰ.用高锰酸钾制备
资料一:(1)3K2MnO4+2H2SO4═2KMnO4+MnO2↓+2K2SO4+H2O
(2)K2MnO4易溶于水
实验室加热高锰酸钾制氧气,反应的化学方程式为 。其反应类型是 。将反应后的固体剩余物用稀硫酸浸取一段时间后过滤、洗涤、烘干即得MnO2,用稀硫酸而不用水浸取的原因是 。
Ⅱ.用硫酸锰制备:电解MnSO4溶液可制得活性MnO2,同时生成氢气和硫酸,该反应的化学方程式为 ,一段时间后溶液的pH将 (填“变大”、“变小”或“不变”)
Ⅲ.用废锂电池制备
资料二:2Al+2NaOH+2H2O═2NaAlO2+3H2↑
用废锂电池正极材料(LiMn2O4、碳粉等涂覆在铝箔上)制备纳米MnO2,并进行锂资源回收,流程如下:

请回答下列问题:
(1)“滤液”中溶质的主要成分是 (填化学式)。
(2)在实验室进行“过滤”操作时,需要的玻璃仪器有烧杯、漏斗和 。
(3)MnO2与碳粉经下列三步反应制得纳米MnO2:
①2MnO2+C  2MnO+CO2↑
2MnO+CO2↑
②MnO+H2SO4═MnSO4+H2O
③3MnSO4+2KMnO4+2H2O═5MnO2↓+K2SO4+2H2SO4
上述涉及元素化合价变化的反应有 (填序号)。
IV.用碳酸锰制备
控制一定的温度,焙烧MnCO3制取MnO2的装置如下:

(1)实验中观察到澄清石灰水变浑浊,写出石英管中发生反应的化学方程式 。
(2)MnCO3在空气中加热易转化为锰的不同氧化物,其残留固体质量随温度的变化如图所示。图中B点对应固体成分的化学式为 (请写出计算过程)
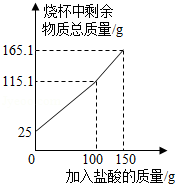
某化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,进行了如下实验:取25.0g洗净、粉碎后的鸡蛋壳样品放于烧杯中,向烧杯中滴加稀盐酸(整个过程不考虑盐酸的挥发和气体的溶解),实验测得烧杯中剩余物质的质量与加入盐酸的质量之间的关系如图所示:求:
(1)产生CO2的总质量为 g。
(2)鸡蛋壳中碳酸钙的质量分数。
小明在登山的过程中发现山上的岩石是红色的,他根据所学知识猜测岩石中可能含有氧化铁,为了验证猜想并到测定其含量,小明进行了以下探究:
【查阅资料】
①一定温度下,CH 4可将Fe 2O 3还原为单质铁,若温度控制不当,还可生成少量的Fe 3O 4.②单质铁和Fe 3O 4均能被磁铁吸引。
【实验探究】
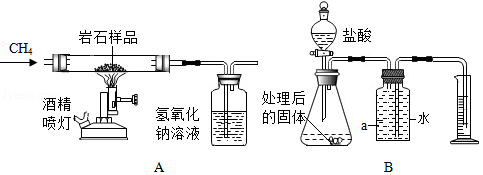
(1)小明利用A装置进行实验。在点燃酒精喷灯之前先通入一段时间CH 4,目的是 。
(2)小明将A装置中得到的固体经过水洗、过滤、干燥处理后,再通过B装置进行实验,观察到仪器a中的现象为 ,从而得出了岩石中含有氧化铁的结论。
(3)小明将反应后的B装置冷却到室温,根据量筒内水的体积V(产生气体的体积),通过有关计算求出了岩石中氧化铁的质量分数。
【评价反思】
实验后小明经过认真反思,认为:
(1)在实验中对甲烷的使用没有"物尽共用",请你给出一条合理建议: 。
(2)若B装置的固体含有一定量的Fe 3O 4,则会导致测得的岩石中氧化铁的质量分数比实际含量 (填"偏高"、"偏低"或"不变"),请你利用处理后的固体,CuSO 4溶液、磁铁等试剂及用品,结合资料所给信息,设计实验证明是否含有Fe 3O 4 ;
实验技能训练中,小亮同学向氧化铜和稀硫酸充分反应后的废液中加入一定量的氢氧化钠溶液,发现无明显现象。小亮同学在老师的指导下对氧化铜和稀硫酸充分反应后的废液进行了实验:他分别取50g废液,并向其中逐渐加入等浓度的氢氧化钠溶液,三组实验的数据与图象如下:
|
实验组数 |
第一组 |
第二组 |
第三组 |
|
加入氢氧化钠溶液质量/g |
50 |
100 |
80 |
|
产生沉淀的质量/g |
0.98 |
2.94 |
2.94 |
请根据以上信息回答下列问题:
(1)氧化铜粉末与稀硫酸反应的现象为 。
(2)废液中的溶质有 (填化学式),并计算废液中硫酸铜的溶质质量分数。(写出计算过程)
(3)若三组数据中,只有一组加入的氢氧化钠溶液与废液恰好完全反应,则上图中a的数值为 。

某兴趣小组计划对空气成分进行探究,以下是他们的实验设计方案:

(1)除去二氧化碳和水蒸气:图1中装置B的作用是 ,装置A、B顺序能否颠倒 (填“能”或“否”)。

(2)除去氧气:该小组根据教材中拉瓦锡研究空气成分的实验原理,除去了(1)中得到的气体中的氧气。在拉瓦锡的经典实验中(装置如图2),使用汞的优点有 。
A.汞为液态,在加热的条件下只与氧气反应且生成物为固体
B.时间足够长,能将密闭装置中的氧气几乎耗尽
C.无法观察装置中气体体积的变化
D.得到的氧化汞粉末加热生成的气体体积+剩余气体体积=原空气体积
(3)分析误差:该小组按设计方案得到的氮气密度(假设要除去的气体均已除净)与氮气的实际密度有误差,产生误差的原因是 。
(4)拓展与延伸:实验室如何制取氮气呢?
请阅读资料并回答下列问题:
资料:
1.重铬酸铵为桔黄色粉末,加热至180℃时可分解得到氮气;
2.氮气的化学性质不活泼,常温下很难跟其他物质发生反应。但在高温或点燃条件下可与某些物质反应,如:镁能够在氮气中燃烧。
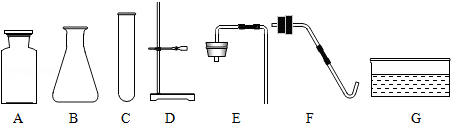
①仪器B的名称是 。
②利用上述仪器和重铬酸铵在实验室制取少量氮气,其发生装置应选择的仪器有 (填序号),还必须补充的一种仪器是 。若用上述装置制氧气,反应的化学方程式为 。
③根据已有知识,收集氮气只能用 法,理由是 。该小组欲进行镁在氮气中的燃烧实验,现收集一瓶含水约 体积的氮气,该如何操作 。
体积的氮气,该如何操作 。
下列有关化学实验的做法,错误的有
A.给试管里的液体加热时,试管里的液体体积不应超过试管容积的
B.滴瓶上的滴管使用后必须清洗,以免污染整瓶试剂
C.除易潮解、有腐蚀性的药品外,可将药品直接放在托盘上称量
D.稀释浓硫酸时,将浓硫酸缓慢注入盛有水的量筒中,并不断搅拌
E.用氢氧化钠固体或浓硫酸进行实验时,最好戴防护眼镜
F.量筒读数时,拿稳量筒,视线应与凹液面的最低处保持水平