许多科学家发现从重视微小差异开始,科学家瑞利和拉姆塞正是重视氮气密度的微小差异,才最终发现了稀有气体氩气。
材料一:1892年瑞利发现,在相同条件下,由空气中除去氧气、二氧化碳、水蒸气和灰尘后获得的氮气,其密度为1.2572克/升;由含氮化合物反应并除去水蒸气后获得的氮气(NH4NO2≜N2↑+2H2O),其密度为1.2505克/升。两者密度差值虽小,却完全超出了实验误差范围。
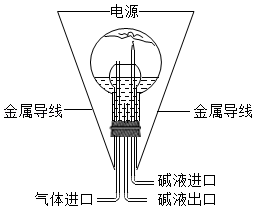
材料二:1894年4月瑞利和拉姆塞开始用如图装置进行“清除空气中氮气”的实验研究:在倒立圆底烧瓶内引入两根金属导线,通电使瓶中空气中的氧气和氮气生成氮的氧化物,用碱液来吸收生成的氮的氧化物和原有的二氧化碳气体。并从气体进口不断向瓶内补充氧气,使反应持续进行。
材料三:瑞利和拉姆塞又设计了另一实验装置,将上述实验所得的气体干燥后,通过红热的铜粉来除去其中的氧气,得到少量的剩余气体。对剩余气体做光谱分析得知,这是一种未知的气体,并测得其密度约是氮气的1.5倍。1894年8月13日他们共同宣布:发现了一种未知气体,并命名为氩气。
材料四:1889年拉姆塞等人利用不同物质沸点不同,又发现了氪气、氖气、氩气。
根据上述材料,回答下列问题:
(1)与纯净氮气密度值更接近的是由 获得的氮气密度值(填“空气中”或“含氮化合物反应”);
(2)实验中不断向瓶内补充氧气的目的是 ;
(3)在当时实验条件下,很难利用化学反应除去氩气,获知“未知气体”中还有其他气体存在,其理由是 。
请沿用科学家认识事物的方法认识"空气"。
(1)从分类角度:空气属于 (填"混合物"或"纯净物")
(2)从微观角度:用"  "表示氮原子,"
"表示氮原子,"  "表示氧原子。
"表示氧原子。
①用"  "可表示的微粒是 (填名称)。
"可表示的微粒是 (填名称)。
②同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计。图中可表示空气微观模型的是 (填标号)。

(3)从变化角度:
已知:常温下,氮气沸点﹣196℃,氧气沸点﹣183℃.将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是 。该烧杯放置一段时间后,液态物质剩余约 体积,其主要成分是 。
(4)从应用角度:利用空气制取氮肥的流程如图所示。

①Ⅰ中参加反应的单质甲为 。
②Ⅱ中反应的化学方程式为 。
③物质所含元素化合价发生变化的反应称为氧化还原反应。反应Ⅲ (填"属于"或"不属于")氧化还原反应。
(5)从环保角度:下列保护空气措施合理的有 (填标号)。
A.工厂通过加高烟囱直接排放废气
B.推广使用乙醇汽油代替普通汽油
C.提倡步行、骑自行车等"低碳"出行方式。
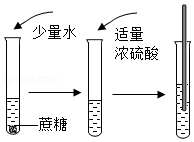
如图“黑面包”实验中,蔗糖(C12H22O11)变黑,体积膨胀,变成疏松的炭,放出有刺激性气味的气体。
[提出问题]改变糖的种类、浓硫酸的体积、水的滴数和温度是否会影响实验效果呢?
[进行实验]分别取5g糖粉进行实验,根据前2min的现象对实验效果进行评分,记录如下:表1实验记录。
|
实验 |
糖 |
浓硫酸体积/mL |
水的滴数 |
温度/℃ |
效果得分 |
|
1 |
蔗糖 |
4 |
5 |
22 |
65 |
|
2 |
蔗糖 |
5 |
10 |
30 |
81 |
|
3 |
蔗糖 |
6 |
15 |
50 |
93 |
|
4 |
冰糖 |
4 |
10 |
50 |
91 |
|
5 |
冰糖 |
5 |
15 |
22 |
88 |
|
6 |
冰糖 |
a |
5 |
30 |
75 |
|
7 |
葡萄糖 |
4 |
15 |
30 |
0 |
|
8 |
葡萄糖 |
5 |
5 |
50 |
0 |
|
9 |
葡萄糖 |
6 |
10 |
22 |
0 |
[处理数据]分析表1,计算效果得分均值,结果如下:
表2效果得分均值
|
因素 |
糖 |
浓硫酸体积/mL |
水的滴数 |
温度/℃ |
||||||||
|
蔗糖 |
冰糖 |
葡萄糖 |
4 |
5 |
6 |
5 |
10 |
15 |
22 |
30 |
50 |
|
|
均值 |
79.7 |
84.7 |
0 |
52.0 |
56.3 |
56.0 |
46.7 |
57.3 |
60.3 |
51.0 |
52.0 |
61.3 |
依据均值推断最佳实验方案,均值越高,效果越好。
[解释与结论]
(1)蔗糖变成黑色的炭,发生了 (填“物理”或“化学”)变化。
(2)推测放出的气体含SO2,从元素守恒角度说明理由: 。
(3)实验6中,a为 mL。
(4)根据表2推断,“黑面包”实验最好选择5g冰糖、5mL浓硫酸、 滴水和50℃。
[反思与评价]
(5)表2中,22℃对应的均值为51.0,计算该值所依据的3个数据分别是 。
(6)综合分析,使实验3的效果得分高于实验4的因素有 。
请从A~D中任选三个作答,若均作答,按前三个计分。如图,在一只烧杯中进行实验。补全实验方案。
|
序号 |
目的 |
步骤 |
|
A |
探究 |
①加入NaOH溶液; ②滴加酚酞溶液;③加入适量盐酸 |
|
B |
检验NaCl中混有Na2CO3 |
①加入少量样品;②加入适量水至全部溶解; ③加入 |
|
C |
验证KCl不能无限溶解 |
20℃时,①加入100g水; ②加入18g KCl; ③加入 (已知:20℃时,KCl的溶解度为34g) |
|
D |
配制 。 |
①加入2.5gNaCl; ②加入47.5g水; ③搅拌至全部溶解 |
用图1装置进行实验,先后将溶液快速全部推入,测得一段时间内压强变化如图2所示。
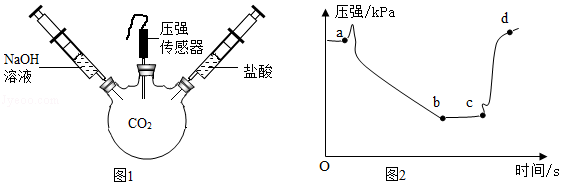
(1)先推入的溶液是 。
(2)bc段压强不变,原因是 。
(3)cd段压强变大,用化学方程式解释: 。
用粗木棍在涂有蜡的锌板上写“明”“和”两个字,露出下面的锌板。向“明”字上滴加CuSO4溶液,向“和”字上滴加盐酸。
(1)“明”字上的现象是 。
(2)“和”字上产生气泡,用化学方程式解释: 。
