实验室有一变质的氢氧化钠样品(样品中只含碳酸钠杂质,且成分均匀),为测量样品中Na 2CO 3的质量分数,小明进行了如下实验。
①取质量、大小相同的3个烧杯,分别加入一定质量分数的稀盐酸100克;
②向上述3个烧杯中分别加入3份质量不同的样品;
③充分反应后,再用电子天平称量烧杯及烧杯内物质的总质量(假设产生的气体完全逸出)。实验数据如下:
实验一 |
实验二 |
实验三 |
|
反应前稀盐酸+烧杯质量(克) |
150 |
150 |
150 |
反应前固体样品质量(克) |
4 |
8 |
12 |
反应后烧杯内物质+烧杯质量(克) |
m |
155.8 |
158.7 |
已知实验中发生的化学反应:NaOH+HCl═NaCl+H 2O
Na 2CO 3+2HCl═2NaCl+H 2O+CO 2↑
(1)分析表中数据,写出判断实验二中的样品已完全反应的理由: 。
(2)表中的m值为 。
(3)根据实验二中的数据计算样品中Na 2CO 3的质量分数。

盐水选种是我国古代劳动人民发明的一种巧妙的挑选种子的方法.农业生产上常用质量分数为15%﹣20%的氯化钠溶液来选种.
(1)要配置150kg16%的氯化钠溶液,计算应称取氯化钠的质量.
(2)选种进行一段时间后,农技员估计溶液和溶质质量分数都有所减少,他取出50g氯化钠溶液,加入过量AgNO3溶液,得到沉淀14.35g,计算氯化钠溶液中溶质的质量分数.
(3)若此时氯化钠溶液的质量只剩下100kg,要使溶液质量和溶质质量分数都恢复到(1)中的状态,计算需要加入的氯化钠和水的质量.
宇宙飞船内,宇航员所呼出的气体要通过盛有氢氧化锂(LiOH)的过滤网,以除去所含的二氧化碳,其反应方程式为:2LiOH+CO2=Li2CO3+H2O.若过滤网内含有氢氧化锂96g,计算最多可吸收二氧化碳的质量.
侯氏制碱法的核心反应原理如下:NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3
某温度下,向溶质的质量分数为20%的氯化钠溶液47.25g中通入一定量氨气(NH3)和二氧化碳.充分反应后,将溶液中析出的碳酸氢钠晶体过滤,低温烘干,称量,质量为4.4g.计算需要通入氨气的质量.(已知:该温度下碳酸氢钠饱和溶液中,碳酸氢钠与水的质量比为1:9;且溶液中若存在其它溶质,不会对上述比值产生影响).
过氧化氢溶液在存放过程中会自然分解,使溶质质量分数减小.某同学使用一瓶原标注为30%的过氧化氢溶液完成制取氧气的实验.通过称量,该瓶中共有116.8g溶液,取出13.6g在一定条件下进行实验,发现生成气体的质量与反应时间的关系如图所示.试计算
(1)现在这瓶过氧化氢溶液的溶质质量分数.
(2)该瓶溶液中,已经分解的过氧化氢质量.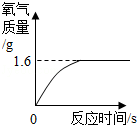
燃烧含硫的煤或燃放鞭炮都会产生污染空气的二氧化硫气体.完全燃烧4g硫,计算生成二氧化硫的质量.