化学就在我们身边,通过一年的学习,我有了许多收获:
(1)我认识了许多化学之最(用化学用语回答)
①空气中含量最多的气体单质是 ;
②最简单的有机物 ;
③地壳中含量最高的金属元素 。
(2)我知道了许多鉴别物质的方法。
①我会用 鉴别软水和硬水。;
②我会用 鉴别二氧化碳和一氧化碳;
③我会用 法来鉴别合成纤维制品和羊毛制品。
CO俗称“无形杀手”用物质X可以测定空气受CO污染的程度,X与CO反应的化学方程式为:X+5CO=I2+5CO2根据生成CO2的质量,可测定CO的含量,请写出X的化学式 .
已知碘元素符号为I,它的原子结构示意图如图.请结合所学知识填写:
X的值为 ;
碘元素的化学性质与下列哪种元素的化学性质最相似? .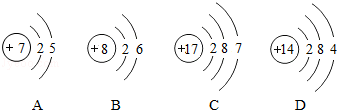
水是人类生活中不可缺少的物质.
下列净水方法中,通常用于除去水中难溶性杂质的是 ,净水程度最高的是
| A.过滤 | B.煮沸 | C.蒸馏 | D.吸附 |
自来水厂常用二氧化氯消毒,其中氯元素的化合价为 ;
自来水中含有少量Ca2等可溶性化合物,烧水时Ca2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一.请写出Ca2受热分解的化学方程式: .
有经验的鱼民在进行长途运输鲜鱼的过程中常常在水中加入少量的过氧化钙固体.已知过氧化钾的化学式可表示为K2O2,则其中氧元素的化合价为 .则过氧化钙的化学式为 .若过氧化钾与水反应的方程式表示为2K2O2+2H2O═4KOH+O2↑,则过氧化钙与水的反应方程式 .请说出使用过氧化钙可以使鱼长期存活的理由: .
为降低汽车尾气对大气的污染,以优美的城市环境迎接2008年的北京奥运,北京市有关部门拟用乙醇替代液化石油气作为公交车的燃料.
以前的汽车燃料不充分燃烧时,会放出大量的有害物质.如: 、 ;
乙醇燃烧时反应的化学方程式为: .