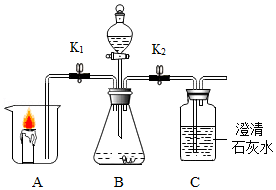
根如据图所示装置完成实验,并按要求填写表格内容。
关闭K2 打开K1 A中现象 |
B中发生反应化学方程式 |
解释A 中现象 |
关闭K1 打开K2 C中现象 |
用化学方程式解释C中现象 |
蜡烛熄灭 |
|
|
|
|
蜡烛燃 烧更旺 |
|
|
|
请根据下列装置,回答问题: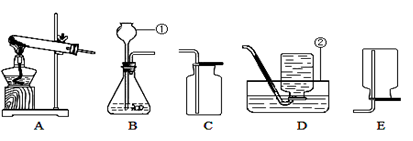
(1) 写出标号①②的仪器名称:①,②。
(2) 实验室制取CO2可以选择的发生装置是(填写装置序号),反应的符号表达式为是。
(3) 若要收集较纯净的O2,可选用的收集装置是(填写装置序号)。若用C装置收集O2,要判断O2是否集满,可将,(填一操作),若看到现象,则标明氧气已经收集满了。
(4)选用A装置加热高锰酸钾方法来制取氧气,细心的同学发现试管的导管口缺少了一团棉花,放棉花的作用是。若同时采用D装置来收集氧气,则实验结束的时候应该先将,再,否则水槽内的冷水会倒流,试管破裂。
(5)一氧化氮是大气污染物,但少量NO在人体内具有扩张血管、增强记忆的功能。实验室收集NO只能用排水集气法。据此我们推测出认为NO具有的性质是。
(答出一点即可,但不可回答NO是一种气体)
(6)将B装置改成I装置,通过拉动铜丝可以控制底部破损的小试管升降.这一改进的主要目的是____(选填序号);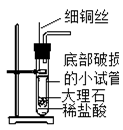
A.使反应随时发生或停止
B.使破损的小试管得到利用
C.生成更多的CO2
(7) 加热固体碳酸氢铵能产生CO2,其符号表达式是:。
他不选用碳酸氢铵制取CO2的理由是。
(8)常温下,乙炔是一种无色气体,密度比空气略小,难溶于水。实验室常用碳化钙固体与饱和食盐水反应来制取乙炔。现选择合适的装置来制取并收集乙炔,应该选择的发生装置是_____(填序号,下同),收集装置是_________。若用乙图装置收集乙炔(瓶内预先装满水),乙炔应从______端进入(选填“A”或“B”)。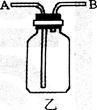
完成下列变化的符号表达式,并按要求填空。
(1)实验室用双氧水制取氧气(二氧化锰粉末作催化剂):.
(2)实验室加热高锰酸钾制氧气的反应:,基本反应类型为反应。
(3)镁带在氧气中燃烧:,军事上利用镁可用作。
(4)二氧化碳通入含有紫色石蕊的水中:,基本反应类型为反应。
(5)铁丝在氧气中燃烧:,若将氧气换成空气,则该化学反应不能进行,其原因是。
(6)二氧化碳通入澄清石灰水:。
(8分) 水是生命之源,也是人类最宝贵的资源。用你学过的化学知识回答下列问题:
(1)欲除去水中不溶性杂质,需进行过滤操作,该操作过程中玻璃棒所起的作用是。
(2)硬水中含有较多可溶性钙、镁化合物,硬水会给生活和生产带来许多麻烦。区分软水和硬水常用的物质是 ,生活中可用来降低水的硬度。
(3)根据下图回答下列问题。
① 试管A中的气体的名称是,写出电解水反应的符号表达式,该实验证明水是由
两种元素组成的。
(4) 淡水资源有限,要节约用水,你认为可采取哪些节水措
施(举1例)?。
下面是对金属钠性质的描述:① 密度比水小;② 熔点低;③ 有银白色金属光泽;④ 常温下能与水剧烈反应;⑤ 常温下易被空气中的氧气氧化。
用序号回答:属于物理性质的是,属于化学性质的是。据上述性质推测,金属钠(填“能”或“不能”)在空气中燃烧。
(1)化学世界绚丽多彩,请选择适当的序号填空。
| A.绿色 | B.黑色 | C.紫黑色 | D.白色 |
| 物质 |
高锰酸钾固体 |
氧化镁 |
四氧化三铁 |
碱式碳酸铜 |
| 颜色 |
(2)形态各异的物质可按一定规律分类。现有下列物质:
A 氧气 B 稀有气体 C 冰水共存物
D含碘盐 E.洁净的空气 F.液氧
请选用各物质名称前的字母序号填写:属于混合物的是。