A~F是六种常见的物质,分别由H、O、C、Cl、Ca五种元素中的两种或三种组成,请回答下列问题:
(1)A是一种氧化物,可用作干燥剂,A与C反应能生成E,A的俗称为 。
(2)B、C常温下均为液体,且组成元素相同,B在一定条件下可生成C,B的化学式为 。
(3)对NaOH溶液依次进行实验,现象如图所示:
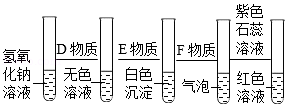
①D和E两种物质分别是 、 (写化学式)。
②加入F的溶液后,沉淀溶解并产生大量气泡,用化学方程式表示产生此现象的原因 。
③最后得到的红色溶液中含有的物质有水、石蕊、 ,下列离子不能与该溶液中的离子共存的是 。
﹣ 2+ 32﹣ 3﹣。
二氧化碳是一种宝贵的碳氧资源.一定条件下,二氧化碳转变成燃料甲醇(CH3OH)的化学方程式为CO2+3H2 CH3OH+H2O.若生产64t甲醇,则可回收二氧化碳多少吨?
探究过氧化氢分解的影响因素.

(1)王老师使用压强传感器等设备,检测不同温度下过氧化氢分解时气体压强如图所示的压强﹣时间的曲线变化.由此可知,其它条件一定时.温度越高,过氧化氢的分解速率 (填“越快”、“越慢”或“不变”);
(2)请你设计实验方案,探究浓度对过氧化氢分解速率的影响(写出简要的实验步骤) .
认识仪器、选用装置以及正确处理实验意外,是实验素养的具体体现。
(1)图1为实验室制备气体常用的发生装置。仪器a的名称是 ;
(2)1773年,瑞典化学家舍勒用图2所示装置制备氧气,在曲颈瓶中装有硝酸钾和浓硫酸的混合物,置于火炉上加热,产生的氧气用动物膀胱收集。该实验若改用图1中的发生装置,最合适的是 (填装置下面的字母);
(3)小明用高锰酸钾制备氧气,实验结束时,先熄灭酒精灯,导致水槽中的水倒流进入了导气管。可采用的补救措施是 (说出一种)。
某实验小组做中和反应的实验,向盛有氢氧化钠溶液(滴有酚酞试液)的烧杯中逐滴加入稀盐酸,并不断搅拌。如图为依据实验数据绘制的 V(盐酸)﹣pH图。
(1)滴加盐酸的体积为V1时,溶液呈什么颜色?
(2)滴加盐酸的体积为V2时,溶液中除了水分子外,主要的微粒有哪些?
(3)举出中和反应的一个应用实例。

2017年5月,我国首次海域可燃冰(主要含有甲烷水合物)试采成功,实现了历史性的突破.请回答:
(1)CH4中碳元素与氢元素的质量比;
(2)可燃冰作为能源的一个优点.