现有一包白色粉末,可能由氯化钾、氢氧化钠、硝酸钠和硫酸铜中的一种或多种物质组成。为确定其成分,某兴趣小组同学进行了如下探究。
(1)甲同学通过观察颜色,认为该粉末中不含硫酸铜,他是根据物质的 性质得出该结论的;乙同学认为甲同学的方法不能确定粉末中不含硫酸铜。
(2)他们设计并进行了如下实验:(已知Ag2SO4微溶于水)

①写出生成蓝色沉淀的化学方程式 ;
②通过以上实验,该白色粉末中可能含有 ;
③加入过量Ba(NO3)2溶液和稀硝酸的目的是 。
水对人类生活、生产有着重要意义。
① 图一是某自来水厂的净水过程示意图,其中活性炭的作用是 (1),常用的消毒剂是 (2)。
② 18世纪末,在前人探索的基础上,法国化学家拉瓦锡通过水的生成和分解实验研究确定了水的组成。图二是电解水的装置,试管a中的气体是 (3)。将a、b中的气体混合,如图三所示点燃,发出尖锐的爆鸣声,试管内壁出现小液滴,该液体是 (4) (填化学式)。
③ 水是一种良好的溶剂,生活中经常把溶于水的物质配成溶液使用。葡萄糖注射液是医院中常用的药品。葡萄糖(C6H12O6)由 (5) 种元素组成,每个C6H12O6分子中含有 (6) 个原子,C6H12O6中H的质量分数是 (7) (精确到0.1%)。
人类生存离不开空气。
① 日常生活中燃料燃烧是与空气中的 (1) 发生的化学反应。化石燃料燃烧产生的SO2、CO2、粉尘等物质带来很多环境问题,例如,引起酸雨的主要物质是 (2) ,引起温室效应的物质是 (3) 。工业上可以用氢氧化钙悬浊液吸收SO2生成CaSO3白色沉淀,该反应的化学方程式是 (4) 。
② 右图是研究空气组成的实验。足量红磷燃烧产生大量的白烟,这是生成的 (5) (填化学式)。红磷熄灭后冷却至室温,打开止水夹可以观察到 (6) ,剩余气体是 (7) (填“纯净物”或“混合物”)。
已知天然气的主要成分是甲烷,通常情况下甲烷是一种无色、无味、难溶于水、密度比空气小的气体,请回答下列问题:
(1)甲烷作为一种优质燃料,在空气中完全燃烧的化学方程式_______________________
(2)假如采用如图所示装置收集甲烷,则气体入口为________________________________
(3)若用该装置并用排水法收集甲烷时,其操作为__________________________________
某化合物在氧气中完全燃烧时,消耗了氧气4.8克,同时只生成4.4克的二氧化碳和2.7克水,则该化合物的质量为_________克,此化合物所含元素为________________(填:元素符号)各元素的质量比为_________________(与所填元素对应)
右图是 A、B、C三种物质的溶解度曲线,回答下列问题: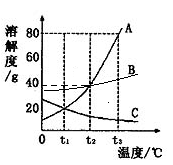
(1)t3℃时,A的溶解度溶解度为
(2)________℃时,A、C的溶解度相等.
(3)如果A物质中混有少量B物质,可用的方法得到较纯
的A物质。
(4)在t2℃时,将200gB物质的饱和溶液蒸发10g水,可析出晶体B(不含结晶水)g。
(5)t2℃的等质量A、B两种物质的饱和溶液分别降温到t1℃析出晶体多的是___________物质。
(6)在t2℃时,向50克的水中加入25克A物质,充分溶解后所得的溶液为_____________(填“饱和溶液”或“不饱和溶液”),形成溶液的溶质质量分数_________。