工业上常用熟石灰(主要成份:Ca(OH) 2)和纯碱(主要成份:Na 2CO 3)混合加工制取烧碱(化学式:NaOH)。请问:工业上制取40吨烧碱,需要消耗含Na 2CO 3质量分数为90%的纯碱多少吨?(计算结果保留一位小数)
(7分)实验室废液桶中收集到大量含有的盐酸与氯化钙的的废液(不考虑其他杂质)。同学们测定该废液中含氯化钙的质量分数,他们取100g废液向其中慢慢滴加质量分数为26.5%的Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示。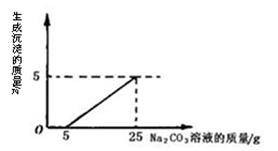
(1)在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成的原因是。
(2)求废液中含氯化钙的浓度。
(3分)在发生重大灾害时,为防止灾区的病菌传播,防疫人员大量使用了“漂白粉”来杀菌消毒,“漂白粉”的有效成分为次氯酸钙[化学式为:Ca(ClO)2]。请回答:
(1)次氯酸钙中氯元素的化合价为。
(2)次氯酸钙中氯元素的质量分数是(精确到0.1%)。
(3)若灾区饮用水每50kg至少需要漂白粉250g,则消毒一桶水(约20kg)至少须加漂白粉g。
7.0g含杂质的铁粉样品与足量稀硫酸反应,产生氢气的物质的量与时间关系如图所示(杂质不与酸发生反应)。计算样品中所含铁的质量分数(根据化学方程式列式计算)。
某化学兴趣小组在实验室进行木炭还原氧化铜的实验,装置如下图。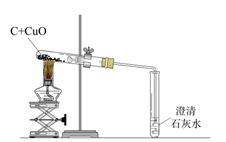
(1)利用小心地将木炭和氧化铜的混合粉末铺放进试管。
(2)将试管固定在铁架台上,试管口略向下倾斜的目的是。
(3)用酒精灯加热混合物几分钟,酒精灯加网罩的目的是,观察到澄清石灰水。然后先撤出导气管,待试管冷却后再把试管里的粉末倒在纸上,观察到的现象是。
(4)要使80g氧化铜完全还原,需要碳的质量至少是多少?(写出计算过程)
Na2CO3中往往会含有少量的NaCl,现在一烧杯中盛有20.4g的固体混合物,向其中逐渐滴加溶质质分数为10%的稀盐酸。放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题:
①当滴加稀盐酸至图中B点时,烧杯中溶液的pH7(填>、=、<)。
②当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常温),通过计算求出其中溶质的质量分数。(计算结果保留一位小数)