对以下事实的解释错误的是
| 事实 |
解释 |
|
| A. |
用氦气充霓虹灯 |
氦气化学性质稳定 |
| B. |
打开可乐瓶盖溢出大量气泡 |
压强减小导致CO2溶解度减小 |
| C. |
活性炭用于净水 |
它有吸附性 |
| D. |
自来水生产过程中使用氯气 |
目的是杀菌消毒 |
将硝酸钾的饱和溶液变为不饱和溶液的方法是
| A.升温 | B.降温 | C.蒸发水 | D.加溶质 |
属于化合反应的是
A.CuO+CO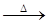 Cu+CO2 Cu+CO2 |
B.NaOH+HCl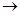 NaCl+H2O NaCl+H2O |
C.3Fe+2O2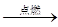 Fe3O4 Fe3O4 |
D.CaCO3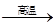 CaO+CO 2↑ CaO+CO 2↑ |
古代“银针验毒”的原理是:4Ag+2H2S+X→2Ag2S +2H2O,X的化学式为
| A.H2 | B.S | C.O2 | D.SO2 |
互为同素异形体的一组物质是
| A.水和双氧水 | B.铜片和铜丝 | C.金刚石和石墨 | D.冰和干冰 |