“宏观辨识与微观探析”是化学学科核心素养之一,化学学习要让学生既能够“见微知著”,也能够“见著知微”。
金属钠在氯气中燃烧生成氯化钠,如图为氯化钠形成的示意图。
根据所给信息,请回答:
(1)钠原子的核外电子层数是 ,在化学反应中易 (填“得到”或“失去”)电子。
(2)元素的化学性质主要是由原子的 决定的。
(3)化学反应前后,氯元素的化合价变化为 。
(4)构成氯化钠的离子是 (填微粒符号)。

镁条在空气中燃烧,不仅生成氧化镁、氮化镁,还有少量镁与二氧化碳反应生成另一种单质和镁的氧化物。
(1)已知氮化镁中氮元素的化合价为-3价,请你写出氮化镁的化学式。
(2)写出镁与二氧化碳反应的化学方程式,
指出该反应的基本类型:反应。
(10连云港25)在上海世博园江苏馆的“春华秋实”展区,用我市东海水晶雕出的作品《寄畅园之冬》吸引了众多参观者的眼球。东海县石国家火炬计划硅胶材料产业化基地,产品由晶莹剔透的成分为SiO2)是制取高纯硅的主要原料,高纯硅又是制造计算机芯片的主要原料。
其生产过程示意图如下: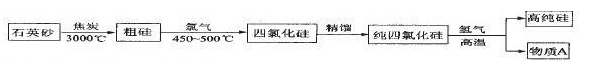
请你自学上述资料后,回答下列问题
(1)由石英砂制得高纯硅的反应原理中,属于化合反应的是填数字代号,下同),属于置换反应的是
(2)粗硅提纯必须在无氧的氛围中进行,除了考虑到硅易被氧化成二氧化硅外,还有一个原因是
(3)生产过程示意图中的“物质A”用水吸收,可得副产品(一种常见的酸)的名称是
(4)作为电器、电子、光纤等行业原料的石英砂纯度要求高,需要对普通石英砂(含有少量的CaCO3、Fe2O3)进行提纯,其中酸洗(用盐酸)和高纯水洗是两个最重要的步骤。请写出酸洗步骤中的一个反应的化学方程式(任写一个);判断高纯水洗是否洗净的方法是:取少量最后的洗涤液于试管中,向其中滴加AgNO3溶液,若无现象,则表明残留物已洗净;否则,表明残留物未洗净。
(3分)如图是密闭体系中某反应的微观示意图,“○”和“●”分别表示不同原子。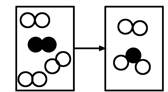
(1)反应后方框内应再填入1个微粒(选填序号)。
A.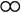 B.
B. C.
C.
(2)该反应所属的基本反应类型是反应。
(3)写出符合该微观示意图的一个具体反应的化学方程式
。
(10揭阳19).(4分)今年我国西南地区地区特大干旱历史罕见。为缓解旱情,政府组织实施了多次人工降雨。利用碘化银进行人工降雨就是利用高炮或飞机,将碘化银炮弹发射到高空云团的零度层以上,利用碘化银在高空中分解生成银单质和碘单质,形成人工冰核。这些冰核经过水汽凝聚,形成冰晶。冰晶发展到一定程度,通过零度层下降之后形成降雨。另查资料知:碘的元素符号为I,其常见化合价为-1,化学式为I2
(1)写出碘化银分解的化学方程式:;
(2)写出另外一种可用于人工降雨的物质名称;
(3)请你提出一个解决水危机的预防性方案:。