为测定某氧化铜和铜的固体混合物中氧化铜的质量分数,小勇同学取20g固体混合物置于烧杯中,将100g稀硫酸分为四等份依次加入其中进行实验,测得数据如下:
次序 |
① |
② |
③ |
④ |
加入稀硫酸的质量/g |
25 |
25 |
25 |
25 |
剩余固体的质量/g |
16 |
a |
10 |
10 |
回答下列问题:
(1)原固体混合物中,氧化铜的质量分数为 。
(2)上表中,a的值为 。
(3)计算该实验所用稀硫酸中溶质的质量分数。(写出计算过程,结果精确到0.1%)
思维模型是依据事物发展内在规律所建立的解决问题的基本框架,能引导有序思维、增进深度理解、促进问题解决。小科建构了“混合物提纯”的思维模型:
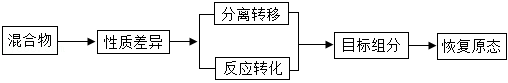
【初步理解】根据混合物组分的性质差异,获得混合物中目标组分。
(1)海水淡化是将海水中的盐与水分开,常压加热蒸馏法是其中的一种:常压下将海水加热形成水蒸气,再液化得到淡水的过程。从建模角度分析,海水加热形成水蒸气属于上述模型中的 (填“分离转移”或“反应转化”)。
【探究本质】根据组分的性质差异,选择合适方法,实现物质提纯。
(2)从含少量氯化钠的硝酸钾固体中提纯硝酸钾,是通过溶解、蒸发浓缩、冷却结晶、过滤、洗涤、干燥实现的。其中过滤操作将硝酸钾晶体与溶液分离是根据 不同。
【实践应用】根据混合物中某组分发生化学反应,提高混合物中目标组分纯度。
(3)小科取10克混有少量硫酸的盐酸溶液,滴入氯化钡溶液至不再产生沉淀,经过滤、洗涤和干燥得到沉淀0.233克,则原混合溶液中硫酸的溶质质量分数为 。
【融合创新】依据科学原理,融合技术与工程,形成新颖而有价值的解决实际问题方案。
(4)常压加热蒸馏法,能耗大、成本高。小科查阅资料获知,现在世界上的许多大型海水淡化工厂,都已经采用低压加热蒸馏法,请解释其蕴含的科学道理 。
某项目学习小组用传感器开展“影响铁锈蚀因素”的探究,设计如图1所示实验装置并完成实验。实验过程中,传感器采集数据绘制得到如图2的甲、乙两幅曲线图。
【资料1】一定条件下,碳和氯化钠溶液可加快铁的锈蚀,但它们本身不参加反应。
【资料2】该实验步骤如下:
①检查装置气密性;
②装药品,将5克铁粉和2克碳粉加入锥形瓶,并加入2毫升饱和氯化钠溶液;
③立即塞紧橡皮塞,橡皮塞上已插有一支装有5毫升稀盐酸的注射器及传感器;
④观察现象,采集数据。

用所学知识及以上资料信息完成下列问题:
(1)实验进行一段时间后,注射器中的盐酸会自动注入瓶内,原因是 ;
(2)图2甲、乙曲线图中, 段温度升高,瓶内压强减小; 段温度升高,瓶内压强增大。解释产生这两个不同现象的原因。
为了保护生态环境,针对全球气候变化,中国政府向全球承诺,力争于2060年前实现“碳中和”。“碳中和”是指在一定时间内,使二氧化碳的排放总量与吸收总量平衡,实现“零排放”。实现“碳中和”通常可采取如下措施:
Ⅰ.碳减排:减少人类生产和生活中二氧化碳的排放量。
(1)下列做法不能实现“碳减排”的是 。
A.加高烟囱排放工业废气
B.推进新能源汽车使用
C.废弃物分类投放并回收利用
D.养成节约用水用电习惯
Ⅱ.碳吸收:①利用植物光合作用,这是自然界消耗二氧化碳的最重要途径;②利用“碳捕捉与封存技术”,即通过一定的方法,将工业生产中产生的 分离出来进行储存。在实际生产中,经常用 溶液来“捕捉” 流程如图所示(部分条件及物质未标出)。
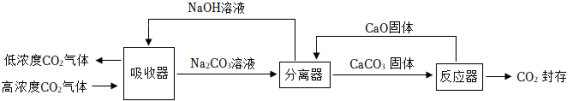
(2)用该技术进行“碳捕获”有效利用了原材料,该过程中被循环利用的物质有 。
(3)分离器中发生的反应:① ,② 。现有溶质质量分数为10.6%的 溶液100千克,求完全反应后,理论上可生成 的质量(要求根据化学方程式计算)。
Ⅲ.碳转化:指二氧化碳的资源化利用。
在化学实验中,经常需要对药品用量进行估算。既能确保实验成功,又能养成节约和环保的习惯。某化学兴趣小组为了体验估算方法,进行了如下实验:
【实验目的】对选定实验中所需药品用量进行估算并验证估算用量足够。

(1)【实验活动一】估算稀盐酸用量
①写出碳酸钙与稀盐酸反应的化学方程式: 。
②取2g石灰石样品进行实验(样品中除碳酸钙外,其余成分既不与盐酸反应,也不溶解于水),请估算,至少需要溶质质量分数为7.3%的稀盐酸 g。
(2)【实验活动二】验证估算的稀盐酸用量足够
方案一:
实验过程如图所示:
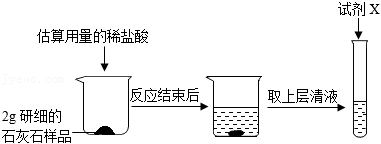
①将石灰石研细的目的是 。
②若图中试剂X为紫色石蕊试液,观察到的现象是 ,说明估算的稀盐酸用量足够。
③为达到与②相同的实验目的,试剂X还可以选择下列试剂中的 (填字母序号)。
| A. |
溶液 |
| B. |
溶液 |
| C. |
溶液 |
| D. |
|
方案二:
④只用以下两种规定用量的药品:2g石灰石样品和估算用量的稀盐酸,设计实验进行验证,请简述实验方案。(实验仪器任选)
|
实验操作 |
实验现象 |
实验结论 |
|
|
|
估算的稀盐酸用量足够 |
从宏观、微观、符号相结合的视角探究物质及其变化规律是化学独特的研究方法。根据所给信息,回答下列问题:
宏观辨识
(1)通过科学探究可以认识化学反应中各物质质量之间的关系,如图实验中,将 溶液滴入锥形瓶中,反应结束后,再次称量,观家到托盘天平的指针 (填“向左”“向右”或“不”)偏转。
微观探析
(2)如图是氢气在空气中燃烧的微观示意图,该反应的基本反应类型为 反应。从微观角度分析,过程I表示分子分解成 的过程。

符号表征
(3)氢化镁( )是一种很有发展前景的贮氢材料,能与水反应生成氢氧化镁和一种常见的气体,反应的化学方程式为: 。请补全该反应的化学方程式并写出补全依据。
依据一:化学反应前后原子的种类和 不变。
依据二: 。
