A~F是初中化学常见物质,它们之间的反应及转化关系如图所示(部分反应物、生成物及反应条件未标出),其中A是一种建筑材料的主要成分,在高温下分解为B和C;通常情况下,C是一种无色气体,可用于生成汽水;E俗称纯碱,D、F都是常见的碱。
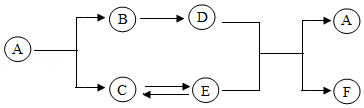
(1)A的化学式是 。
(2)B→D的反应类型是 。
(3)D的一种用途是 。
(4)C与F反应生成E的化学方程式为 。
如图是甲烧在空气中燃烧的微观过程模拟图.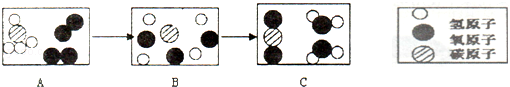
请回答下列问题:
(1)在B中补充画出相关粒子图形,使其表示正确;
(2)补充的依据是;
(3)结合该图示从微观角度解释由B到C变化的实质是.
中新社哈尔滨5月7日电)记者7日从哈尔滨市政府获悉,由于哈尔滨市用煤量增大且气象条件不利于扩散,空气质量曾多次陷入严重污染,该市设原煤禁销区,成为中国首个禁销原煤的城市.这样做目的是,请结合生活实际,给出你的一点建议
韦应物在《观田家诗》中曰:“微雨众卉新,一雷惊蛰始,田家几日闲?耕种从此始.”诗中农民耕种使用的一些工具是由铁合金制成,主要利用其具有 硬度大 的物理性质.“微雨”中雨水的pH约为5.6的原因是,农民种植的玉米给人体提供的营养素是,在种植玉米的过程中需要施用一定量的钾肥.钾肥的作用为.我国古代四大发明之一的黑火药就是利用硝酸钾在点燃条件下与木炭、硫磺剧烈燃烧,瞬间产生大量的热和氮气、二氧化碳,同时产生硫化钾(K2S),其反应的化学方程式为,反应前后氮元素的化合价分别为.
试根据图中信息回答下列问题:
(1)用墨书写的字画能长时间不变色的原因是;
(2)汽车用铅蓄电池中含有的酸为;
(3)煤气的主要成分有;
(4)铁制的水龙头镀铬的目的是.
有A、B、C、D四种元素,已知A元素是地壳中含量最多的元素;B元素的原子内有11个质子,在化学反应中容易失去一个电子;C元素的原子内没有中子,由C元素组成的单质是一种最轻的气体;D元素的原子内共有13个电子,它是地壳中含量最多的金属元素。请根据上述的信息回答下列问题:
(1)请写出这四种元素的元素符号:A是;B是;C是;D是。
(2)B元素的离子结构示意图为:; B元素属于(填“金属元素”或“非金属元素” )
(3)A、C、D三种元素组成的化合物的化学式为:。