为测定某氧化铜和铜的固体混合物中氧化铜的质量分数,小勇同学取20g固体混合物置于烧杯中,将100g稀硫酸分为四等份依次加入其中进行实验,测得数据如下:
|
次序 |
① |
② |
③ |
④ |
|
加入稀硫酸的质量/g |
25 |
25 |
25 |
25 |
|
剩余固体的质量/g |
16 |
a |
10 |
10 |
回答列问题:
(1)原固体混合物中,氧化铜的质量分数为 。
(2)上表中,a的值为 ,实验③所得溶液中的溶质是 (填化学式)。
(3)计算该实验所用稀硫酸中溶质的质量分数。(写出计算过程,结果精确到0.1%)
某化学兴趣小组为探究金属铝和铜的活动性强弱,开展了以下活动。
[查阅资料]
经查阅,金属铝在常温下能与空气中的氧气反应生成致密的氧化铝薄膜。该反应的化学方程式为 。
[对比实验]
|
编号 |
操作 |
现象 |
|
甲 |
将表面未打磨的铝丝浸入CuSO4溶液中 |
无明显现象 |
|
乙 |
将表面打磨后的铝丝浸入CuSO4溶液中 |
铝丝表面析出红色固体 |
|
丙 |
将表面未打磨的铝丝浸入CuCl2溶液中 |
铝丝表面析出红色固体 |
(1)比较实验乙和实验 (填“甲”或“丙”)可得知:打磨能破坏氧化铝薄膜。
(2)实验乙中反应的化学方程式为 ,据此可知金属活动性Al比Cu (填强”或“弱”)。
(3)小明同学对实验丙的现象进行分析,认为H2O对氧化铝薄膜有破坏作用。但此观点马上被其他同学否定,否定的依据是 。
[猜测与探究]
小组同学针对实验丙的现象,经讨论后猜测:Cl﹣破坏了氧化铝薄膜。
为检验此猜测是否正确,他们首先向两支试管中加入相同的CuSO4溶液,并均浸入表面未打磨的铝丝,然后进行了新的探究:
|
操作 |
现象 |
结论 |
推论 |
|
(1)向一支试管中再加入NaCl固体 |
铝丝表面析出红色固体 |
氧化铝薄膜被破坏 |
Na+或① 能破坏氧化铝薄膜 |
|
(2)向另一支试管中再加入Na2SO4固体 |
② |
氧化铝薄膜未被破坏 |
Na+和SO42﹣都不能破坏氧化铝薄膜 |
[结论与反思]
得出结论:前述猜测 (填“正确”或“不正确”)
总结反思:本次探究充分运用了比较法和控制变量法
实验室利用如图所示装置进行相关实验。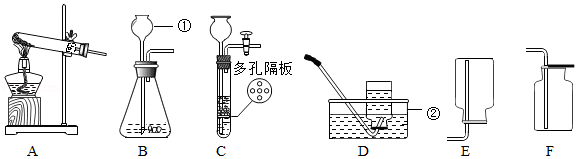
回答下列问题:
(1)写出装置图中标号仪器的名称:① ,② 。
(2)用高锰酸钾制氧气,应选用的发生装置是 (填字母序号),该反应的化学方程式为 ,其中转化为氧气的氧元素与高锰酸钾中氧元素的质量之比是 。
(3)常温下,用锌和稀硫酸反应制取氢气,若要随时控制反应的发生和停止,应选用的发生装置是 (填字母序号),反应的化学方程式为 ;点燃氢气前必须验纯,为确保安全,最好选用装置 (填字母序号)所示方法收集氢气。
钛(Ti)被誉为21世纪的“明星金属”,我国深海探测器“蛟龙”号的耐压球壳由钛合金制造,工业上生产钛的化学方程式为4Na+TiCl4 Ti+4NaCl,现消耗46吨钠,可生产钛的质量为多少?
某化学兴趣小组为探究碱和盐的化学性质,进行了如图1所示实验(忽略空气中CO2对本实验的影响)。请你参与并完成相关内容。
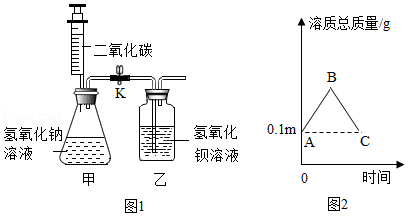
(1)步骤一:关闭K,向下缓慢推动注射器活塞并轻轻振荡锥形瓶,使二氧化碳全部进入锥形瓶,并与m克溶质质量分数为10%的NaOH溶液恰好完全反应转化为碳酸钠,反应的化学方程式为 ,轻轻振荡锥形瓶的目的是 。
步骤二:打开K,向上缓慢拉动注射器活塞,观察到乙中溶液进入甲。
(2)上述实验过程中,甲中溶质总质量变化情况如图2所示, B点对应的溶质总质量为 (用含m的代数式表示,可以不化简)克,BC段反应的化学方程式为 ,BC段溶质总质量下降的原因是 。
(3)步骤一和步骤二结束后,将甲和乙中的物质全部转移到烧杯中,搅拌后过滤,得到白色沉淀和滤液。结合图2中C点的值确定滤液中溶质的成分为 ,理由是 。