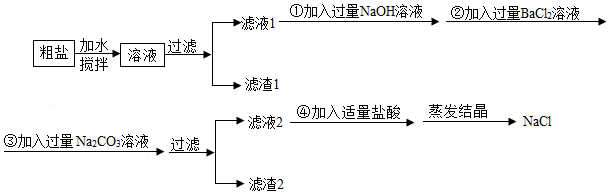
现有一包粗盐,其中含有少量氯化镁、硫酸钠和不溶性的泥沙。为获取纯净氯化钠,设计如图实验方案:
阴离子 阳离子 |
OH﹣ |
Cl﹣ |
SO42﹣ |
CO32﹣ |
H+ |
溶、挥 |
溶 |
溶、挥 |
|
Na+ |
溶 |
溶 |
溶 |
溶 |
Ba2+ |
溶 |
溶 |
不 |
不 |
Mg2+ |
不 |
溶 |
溶 |
微 |
根据上述有关信息回答下列问题:
(1)滤渣1是 。
(2)向滤液1中加入过量NaOH溶液发生反应的化学方程式是 。
(3)滤液2中的溶质除NaCl外还有 (填化学式)。
(4)若④加入的盐酸不慎过量,对氯化钠的纯度 (填“有”或“无”)影响,理由是 。
煤主要含有碳元素,如果把煤的燃烧看作碳与氧气的反应,煤在炉子里的燃烧可能发生的反应有四个:
①C+O2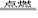 CO2 ②2C+O2
CO2 ②2C+O2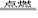 2CO ③C+CO2 高温 2CO ④2CO+O2
2CO ③C+CO2 高温 2CO ④2CO+O2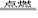 2CO2
2CO2
(1)以上四个反应中,有一个反应不同于其他三个,你的选择是 ,理由是 。
(2)当煤炉里氧气充足时,主要发生①③④反应,在这种条件下,燃烧的碳与消耗的氧气的质量比是 .
(3)当煤炉里氧气不足时,主要发生的反应是:① (填序号)。
泡菜具有独特的风味,适合制作泡菜的食盐水浓度是4%。在配制4%的食盐水2000g时,下列做法:①用80g食盐和2000g水配制溶液;②称量食盐时(1克以下用游码),食盐放在右盘的纸上;③量水的体积时,俯视量筒;④溶解食盐的烧杯内壁是潮湿的 ;其单一错误会导致溶液浓度偏小的是 。
今年某市新增两处4A级景区.初三(1)班的几位同学在周末实地感受了景区的美.
(l)刚进人公园,阵阵花香便扑鼻而来,让几位同学兴奋不已.用微粒观点解释闻到花香是因为_____ ___ ;
(2)随后他们来到了公园天桥,发现坚固的钢材表面喷上了红色漆,在阳光下分外耀眼,同学们感叹:“这颜色真美!”,喷漆的主要目的是为了防止______ ___ ;
(3)他们来到河边,发现河水清澈透明,想要测定该河水的酸碱度,应选用_________
A.石蕊试液 B.酚酞试液 C.pH试纸.
根据下列图文回答问题:
(1)青铜剑属于 (填“纯金属”或“合金”).
(2)高钙豆奶粉的“钙”指的是 (填“元素”、“原子”、或“分子”).
(3)C60分子是由 构成的.
(4)干冰可用于 (填一例).
(5)根据图2中自制汽水的配料回答问题:柠檬酸的pH 7(填“<”、“=”或“>”),能使紫色石蕊溶液变为 色.
现有氢、氧、钠、硫四种元素,选择其中元素写出符合下列要求的化学式:
| 物质类别 |
单质 |
氧化物 |
酸 |
碱 |
| 化学式 |