根据下列装置,结合所学化学知识,回答下列问题:

(1)E图中仪器①的名称是 ;
(2)实验室制取并收集较纯净的氧气,小华同学已选用A装置作为发生装置,则他还需要选择的装置或仪器有 (填装置序号),该反应的化学方程式是 。小华利用上述收集方法收集到的氧气不纯,导致其不纯的原因可能是 (任写出一点);
(3)实验室利用硫化亚铁固体和稀硫酸混合制取硫化氢气体,通常选择的发生装置是 (填装置序号)。这个反应属于复分解反应,对应的化学方程式是 。
已知某固体样品A可能是NH4NO3和MgCO3或两者之一,另有一固体样品B,其中可能含有Na2SO4,BaCl2,CuSO4、KCl四种物质中的一种或多种.按如图所示进行探究实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全反应).
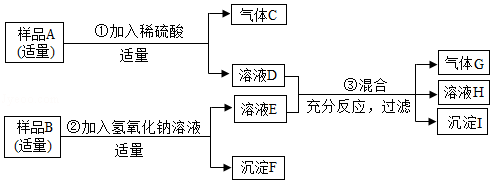
试根据实验过程和发生的现象,填写以下空白:
(1)将气体C通入紫色石蕊试液,试液变 色.
(2)沉淀F的化学式为 .
(3)溶液D中,一定存在的阳离子是 (填写离子符号).
(4)写出步骤③中生成沉淀I的化学方程式 .
(5)在溶液H中,肯定存在的阴离子有 种.
(6)固体样品B中,一定不存在的物质是 (填写化学式),得出此结论的理由是: .
如图所示为实验室中常见气体制备、净化、干燥、收集和进行实验探究的部分仪器(组装实验装置时,可重复选择仪器),某化学小组的同学欲利用其进行下列各化学实验。

(1)以过氧化氢溶液为原料(二氧化锰作催化剂),在实验室中制备并收集干燥的氧气。按照要求设计实验装置,连接仪器,并检验装置的气密性。
①所选装置的连接顺序为 (从左至右填写装置序号字母)。
②制取氧气所发生反应的化学方程式为 。
③下列有关氧气制取和性质的叙述中,不正确的是 (填写序号A、B、C,D之一)
A.实验室制氧气时,应先加入药品,再检査装置的气密性
B.在此反应前后,二氧化锰的质量和化学性质都不发生改变
C.铁丝在纯氧中剧烈燃烧时,火星四射,生成黑色固体
D.氧气是一种化学性质比较活泼的气体
(2)用干燥纯净的氧气对纤维素的组成进行分析探究实验(资料显示纤维素只含C、H、O三种元素)。所选装置按"氧气→D→A→C→碱石灰干燥管"的顺序连接(实验前检验装置的气密性,假设所发生的化学反应都完全充分进行)。装置D的玻璃管中放入纤维素试样的质量为wg,充分反应后,测得装置A的质量增加ag,装置C的质量增加bg,则纤维素中碳元素的质量分数为 (计算结果用含字母的代数式表示)。
若实验中使用的氧气未干燥,这样测算出的纤维素中碳元素与氢元素的质量比与实际值比较将 (填"偏大""偏小""基本一致""无法确定"之一)
(3)用一氧化碳气体(含有少量二氧化碳和水蒸气)测定某铁的氧化物(Fe xO y)试样的元素组成比例,所选装置按"混合气体→A 1→D→C→A 2"的顺序连接(A 1、A 2为浓硫酸洗气瓶,实验前检验装置的气密性,假设所发生的化学反应都充分反应)。进行实验并记录实验数据,如下表所示:
|
装置编号 |
A 1中浓硫酸 |
D中玻璃管内固体 |
C中溶液 |
|
反应前质量 |
150g |
14.4g |
200g |
|
反应后质量 |
152.7g |
11.2g |
213.2g |
①请选择合理数据计算Fe xO y中x:y= (填写最简整数比)。
②从环保角度考虑,该实验方案设计还存在不完善之处,你的具体改进方案是 。
南海是我国的固有领海,蕴藏着丰富的海洋资源。2017年5月18日,我国南海神狐海域的可燃冰试采取得圆满成功,实现历史性突破。
(1)可燃冰的主要成分是甲烷。请你写出甲烧在空气中燃烧的化学方程式: 。
(2)可燃冰被科学家誉为“未来能源”“21世纪能源”,原因是 。
(3)1926年,我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图2所示,试回答下列问题:

①t1℃时,NaCl的溶解度 Na2CO3的溶解度(填写“大于”“等于”“小于”之一)。
②t1℃时,50g水中加入10g Na2CO3,经充分溶解,所得溶液中溶质与溶液的质量之比为 (填最简整数比)。
③t1℃时,将不同质量的碳酸钠饱和溶液和氯化钠饱和溶液均升温至t2℃,此时所得碳酸钠溶液溶质质量分数 氯化钠溶液溶质质量分数(填写“大于”“等于”“小于”“无法判断”之一)。
向100g硫酸铜与硫酸的混合溶液中加入溶质质量分数为10%的氢氧化钠溶液,溶液质量与所加氢氧化钠溶液的质量关系如图所示,回答下列问题:
(1)由图象可知,c点溶液中的溶质是 。
(2)当加入氢氧化钠溶液的质量为80g时,所得不饱和溶液中溶质的质量分数是多少?(结果精确到0.1%)

某小组同学在实验室研究铝与氯化铜溶液的反应,过程如下:
|
实验操作 |
实验现象 |
|
|
①铝片表面附着一层红色固体 ②铝片表面逸出大量无色气体,放出大量的热 ③烧杯底部出现红色固体和白色沉淀 |
(1)打磨铝片的目的是 。
(2)现象①③中的红色固体是同种物质,请写出现象①的化学方程式 。
(3)经检验,现象②中的无色气体为氢气。甲同学猜测可能是氯化铜溶液显酸性,经pH计检验,pH 7,证实了甲的猜想。
(4)探究现象③中白色沉淀的化学成分。
乙同学通过查阅资料认为白色沉淀可能是氯化亚铜(CuCl)。
[查阅资料]CuCl可与浓氨水反应生成无色的Cu(NH3)2+和Cl﹣,Cu(NH3)2+在空气中易被氧化变为蓝色。
[进行实验]①取烧杯底部的白色沉淀,充分洗涤。洗涤的目的是 。
②向白色沉淀中加入浓氨水,沉淀溶解得到无色溶液,将无色溶液分为两份,进行实验:
|
操作步骤 |
实验现象 |
实验结论 |
|
Ⅰ.用试管取其中一份溶液,滴加适量AgNO3溶液 |
产生白色沉淀 |
该溶液中含有
|
|
Ⅱ.将另一份溶液置于空气中一段时间 |
|
该溶液中含有Cu(NH3)2+ |
[得出结论]通过实验可以确定,该白色沉淀是CuCl。
[反思与评价]Al和CuCl2溶液反应为什么会出现CuCl呢。
I.丙同学猜测:可能是Cu与CuCl2溶液反应生成了CuCl.为了验证猜想,他取Cu与15%的CuCl2溶液混合,结果无白色沉淀产生。他又分析了Al和CuCl2溶液反应的实验现象,再次将打磨过的Al片插入盛有15%的CuCl2溶液的试管,并将试管置于冰水中,发现白色沉淀明显减少。于是他将Cu与15%的CuCl2溶液的实验进行了改进,从而证明了Cu与CuCl2溶液反应能生成CuCl,改进的方法是 ,试写出该反应的化学方程式 。
II.丁同学认为丙同学的实验还不够严谨,还应考虑 对Cu与CuCl2溶液反应的影响。