K3[Fe(C2O4)3]•3H2O(三草酸合铁酸钾)为亮绿色晶体。小李和小赵同学在老师的指导下探究K3[Fe(C2O4)3]•3H2O的热分解产物。
[查阅资料]①碱石灰可用于吸收CO2、水蒸气
②含有Fe2+的盐溶液可与K3[Fe(CN)6]发生反应产生蓝色沉淀
③含有Fe3+的盐溶液可与KSCN发生反应生成红色溶液
[提出问题]样品完全分解后,除水蒸气外还生成哪些产物?
[猜想与假设]猜想一:气体产物中含有CO
猜想二:气体产物中含有CO2
猜想三:气体产物中含有
[实验探究]
(1)探究气体产物。
小李同学对气体产物进行探究,设计如图实验(夹持装置及部分装置省略):
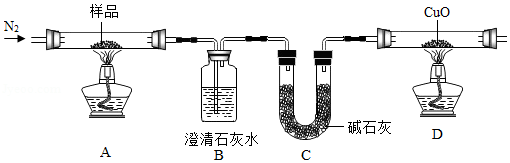
实验中观察到装置B中澄清石灰水变浑浊,装置D中的固体变为红色。由此判断猜想 三 正确。
(2)探究固体产物。
小赵同学对固体产物进行如表探究:取K3[Fe(C2O4)3]•3H2O热分解后的固体产物(经实验证明无磁性)于试管中,加水充分溶解、过滤,再进行如表实验:
实验 |
现象 |
结论 |
|
取滤液加入硫酸 |
① |
固体中含有K2CO3 |
|
取滤渣加入硫酸溶解后,分成两份 |
一份中加入K3[Fe(CN)6] |
② |
固体中含有FeO |
另一份中加入KSCN |
溶液变为红色 |
固体中含有③ 氧化铁 |
|
[实验结论]K3[Fe(C2O4)3]•3H2O的热分解产物有 种。
[拓展延伸]晒制蓝图时,用K3[Fe(C2O4)3]•3H2O作感光剂,其光解反应有FeC2O4生成。432g FeC2O4在一定条件下分解可以得到一种具有磁性的黑色固体和两种含有相同元素的气体,则两种气体质量的最简整数比为 。
工业纯碱中含少量氯化钠。兴趣小组分别采用不同的方法测定工业纯碱样品中碳酸钠的质量分数。
(1)方法一:差量法。称取W克样品与足量的稀盐酸充分反应,生成的二氧化碳通过装有试剂X的乙装置,并利用测量乙装置增加的质量,求得样品中碳酸钠的质量分数。该方法中试剂X可选用 。
(2)方法二:沉淀法。称取15克样品完全溶解于水中配成60克样品溶液,取三个烧杯分三次进行实验,每次加入30克氯化钙溶液充分反应,过滤、洗涤、干燥所得的沉淀质量记录如表。计算样品中碳酸钠的质量分数。
(Na2CO3+CaCl2═CaCO3↓+2NaCl)
|
烧杯1 |
烧杯2 |
烧杯3 |
|
|
样品溶液(克) |
10 |
20 |
30 |
|
氯化钙溶液(克) |
30 |
30 |
30 |
|
沉淀质量(克) |
2 |
4 |
5 |
(3)请写出提高方法一测量精确度的操作建议(写出2条) 。

小明利用稀硫酸与生锈的铁屑反应制取硫酸亚铁,实验流程如图:

资料:①Fe2(SO4)3+Fe═3FeSO4;②硫酸亚铁容易被氧化为硫酸铁等物质。
(1)配制50克溶质质量分数为19.6%的稀硫酸,需溶质质量分数为98%的浓硫酸 克。
(2)写出该实验中的一条化学方程式(除资料①中的反应外) 。
(3)稀硫酸与生锈的铁屑充分反应后,要确保铁有少量剩余,其目的是 。
新冠疫情发生以来,在“坚定信心、同舟共济、科学防治、精准施策”的思想指引下,中国抗疫取得重大胜利!
(1)对新型冠状病毒的毒株分离和基因测序,是研发疫苗和药物的基础。为应对疫情,同学们都居家学习,在此期间做法合理的有 。
A.健康饮食,平衡膳食
B.长时间躺床上看书
C.多服用抗生素增强抵抗力
D.关爱家人,乐观面对生活
(2)佩戴口罩出行是预防新冠肺炎的重要举措。一次性口罩需要及时更换,废弃的口罩应放入 垃圾桶最合适。
(3)对公共场所的定期消毒是控制新冠肺炎的有力保障。“84”消毒液被广泛用于新冠疫情的卫生消毒,可通过氯气与氢氧化钠反应制取,生成物中有氯化钠、次氯酸钠(NaClO) 和水,其中次氯酸钠是消毒液的有效成分。
①次氯酸钠中氯元素的化合价为 。
②写出制取“84”消毒液的化学方程式 。

将12.9克NaCl和Na2CO3固体混合物完全溶于水中形成溶液,再将75克CaCl2溶液分5次加入到该溶液中,充分反应,测得的实验数据如下表。
|
实验序号 |
1 |
2 |
3 |
4 |
5 |
|
加入CaCl2溶液质量/克 |
15 |
15 |
15 |
15 |
15 |
|
生成沉淀的总质量/克 |
3 |
m |
9 |
10 |
10 |
求:(1)表格中m的数值是 。
(2)溶液中Na2CO3完全反应是在第 次实验。
(3)固体混合物中Na2CO3的质量分数。(精确到0.1%)
(4)请画出上述过程溶液中NaCl质量的变化图。

2019年诺贝尔化学奖用于表彰锂离子电池的研发。这种质量轻、可充电、功能强大的电池现在被广泛应用于手机、笔记本电脑和电动汽车等各种产品。

(1)锂电池充电时,电能转化为 能。
(2)碳酸二甲酯(C3H6O3)是锂电池电解液的一种成分,下列关于碳酸二甲酯说法正确的有 。
A.由C、H、O三种元素组成
B.碳元素的质量分数最大
C.相对分子质量是90克
D.分子中C、H、O三种原子的个数比为1:2:1
(3)图为某款锂电池手机在不同温度下的电压随时间变化的图象,请结合图象分析手机夏天比冬天耐用的原因是: 。