请根据下列装置图,回答有关问题:
(1)写出装置图中标号仪器的名称:a 。
(2)实验室用高锰酸钾制取氧气可选用的发生装置是 (填字母),反应的的化学方程式为。
(3)实验室用锌粒和稀硫酸制取氢气的化学方程式为,可选用的收集装置是 (填字母)。
(4)某化学兴趣小组利用B装置并改进后设计了一组“吹气球”实验,装置如图: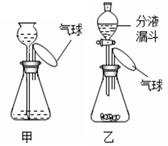
①向甲中长颈漏斗内加水会看到气球胀大,一段时间内气球大小没有变化,该操作的目的是_________。
②若从乙中分液漏斗滴加入少量水入锥形瓶,欲使气球胀大,则锥形瓶中装有的固体物质可以是______。
| A.NH4NO3 | B.NaOH | C.NaCl | D.CaO |
请用化学方程式表示下列反应,并在括号内标明该反应的基本反应类型。
(1)实验室用过氧化氢溶液制氧气()
(2)铜和硝酸银溶液反应()
(3)Al与NaOH溶液反应生成H2和NaAlO2()
(1)运用所学的化学知识回答下列问题。
①防毒面具中使用活性炭,这是利用了活性炭的作用。
②用井水洗衣服时,肥皂不易起泡沫且产生浮渣,该井水是(填“硬水”或“软水”)。
③为了防止水龙头生锈,其表面常镀一层铬,其防锈的原理是。
④用小木棍蘸少量浓硫酸,放置一会后木棍变黑,说明浓硫酸有性。
(2)请从元素C、H、O、N、Na中选择,用物质的化学式填空:
①用作调味品的酸;②最简单的有机物是;
③发酵粉的主要成分是; ④具有挥发性的一种碱。
某化学兴趣小组利用下列装置进行O2、CO2的实验室制法和有关性质的研究。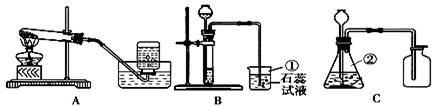
(1)写出下列编号仪器的名称:①_______②______。
(2)甲同学要用KMnO4固体来制取O2,应选用上图中的____装置(填编号);请指出用该装置做高锰酸钾制氧气的缺陷是_____;当O2收集满并取出集气瓶后,停止该实验的正确操作步骤是____。(填“先从水槽中移出导管”或“先熄灭酒精灯”)
(3)乙同学用浓盐酸和石灰石在B装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红。对这一变化的合理解释是_____(填序号)。
A.产生的CO2直接使石蕊试液变红
B.挥发出的氯化氢溶于水使石蕊试液变红
C.产生的CO2与水反应生成H2CO3使石蕊试液变红
(4)丙同学用C装置制取了一瓶氧气,他用向上排空气法收集氧气,验满的方法:_________。
(12 分)射阳县原种场二、三大队紧挨明湖水库,明湖水库坐落县城东部,距入海口18公里,湖长12.3公里,宽400米,平均水深9米左右,总库容3600万立方米,水质较好,是全县人民的饮水源。
(1)小明同学装了一瓶明湖水带回实验室,在老师的指导下,按下列流程制取蒸馏水。
请回答下列问题: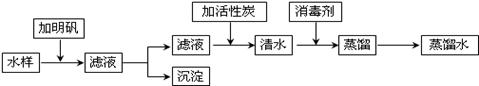
①测定水样的酸碱度,可用____(填“紫色石蕊”、“无色酚酞”或“pH 试纸”)。
②进行过滤操作时,下列做法正确的是____。
A.玻璃棒的一端要靠在三层滤纸的一边
B.漏斗下端的管口要悬放在烧杯的中间
C.滤纸的边缘要低于漏斗口
D.液面不能低于滤纸边缘
③向滤液中加入活性炭,利用其____性,除去水样中的色素和异味。
(2)以下是保护明湖水库的水质的一些做法:
①推广周边居民使用无磷洗衣粉;
②水库周围的工业废水不得排入明湖;
③加快周边居民生活污水集中净化处理的建设;
④周边的农田尽量少用化肥和农药;
⑤为提高经济效益在明湖水库中大量养鱼。
其中合理的是________。(填序号)
(3)下图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:
①P 点的含义是____________。
②t2℃时a、b、c三种物质的溶解度按 由小到大的顺序排列是________(填写物质序号) 。
③t2℃时30ga物质加入到50g水中不断搅拌,所得溶液的溶质质量分数____。
④将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是____(填写选项序号)。
A.c>a=bB.a=b>c C.a>b>cD.b>a>c
(4)根据下表回答:
| OH- |
NO3- |
Cl- |
SO42- |
CO32- |
|
| H+ |
溶、挥 |
溶、挥 |
溶 |
溶、挥 |
|
| Na+ |
溶 |
溶 |
溶 |
溶 |
溶 |
| Ca2+ |
微溶 |
溶 |
溶 |
微溶 |
不溶 |
| Cu2+ |
不溶 |
溶 |
溶 |
溶 |
不溶 |
| Ba2+ |
溶 |
溶 |
溶 |
不溶 |
不溶 |
| Zn2+ |
不溶 |
溶 |
溶 |
溶 |
不溶 |
①BaCO3的溶解性_____。从上表中找出一种不溶碱____(填化学式)。
②Zn(NO3)2、BaCl2两种溶液能不能发生反应?____(填:能”或“不能”)
③利用上表写一个有氢氧化铜生成的复分解反应化学方程式:__________