如图中A~G和M均是初中化学常见物质,①~⑥是初中常见的不同化学反应的编号,A是碳酸氢钠,B、E是组成元素相同的物质,G是铁锈的主要成分,H、M是常见的碱。“→”表示物质间有转化关系,图中部分反应条件和反应物、生成物已省略。请回答下列问题:
(1)写出反应③的化学方程式 。
(2)物质C的化学式是 。
(3)反应①~⑥不涉及的基本反应类型是 反应。

阅读材料,回答问题: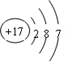
材料1 氯元素(Cl)是一种重要的非金属元素,氯气是双原子分子,在通常情况下为黄绿色气体。
材料2 氯原子的结构示意图如右图,在化学反应中易得到1个电子,达到8电子的稳定结构,氯气化学性质很活泼,具有较强的氧化性,能与多种金属和非金属直接化合,还能与水、碱等化合物反应。
材料3 燃烧不一定要有氧气参加,任何发光、发热的剧烈的化学反应,都可以叫做燃烧,氢气可以在氯气中燃烧生成氯化氢(HCl)。
材料4我国四川5.12地震灾区灾后急需大量消毒剂对灾区饮用水、环境进行消毒,防止灾后疫情发生。氯气可用于制备多种消毒剂、消毒泡腾片,其中二氧化氯是最新一代高效、广谱、安全环保型杀菌消毒、保鲜剂,世界卫生组织(WHO)已将二氧化氯列为第四代A1级安全高效消毒剂。
(1)氯气的化学式为______________,其原子核外电子数为________________。
(2)请总结氯气的有关性质:①物理性质________________________________;
②化学性质________________________________
(3)氯气是一种有毒气体,根据所学化学知识你认为闻氯气的方法是:_______________________。
(4)写出材料3中的化学方程式___________________________________。
(5)写出材料4中二氧化氯的化学式__________________、其中氯元素的化合价为____________。
作为推行“低碳经济”的重要科技进步,太阳能光伏发电成为2010年上海世博会的“亮点”。太阳能光伏发电最关键的材料是高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法。生产流程示意图如下:
(1)三氯甲硅烷(SiHCl3)是由______________种元素组成的混合物。
(2)“精馏”也是蒸馏的一种形式。通过蒸馏可把液体混合物分离开,原理是利用混合物各成分的_____________(填“熔点”或“沸点”)不同。
(3)写出从粗硅到SiHCl3(粗)的化学方程式_______ 。
(4)为了达到绿色化学和资源综合利用的目的,上述生产流程中某些物质可循环使用,这些物质是(填化学式)。
(5)石英砂的主要成分是SiO2,含有少量Al2O3。若要除去石英砂中少量的杂质,可选用的试剂是(填化学式)。
高纯度的CuO可用作颜料、有机合成催化剂等,以下是用粗铜粉氧化法生产高纯度CuO的流程图(说明:所加试剂均过量)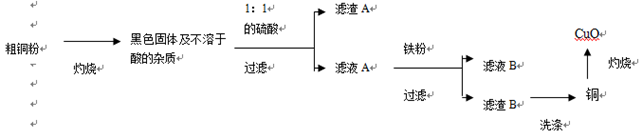
回答下列问题
(1)1:1的H2SO4是用1体积98%的H2SO4与1体积水混合而成,配制该硫酸溶液所需的玻璃仪器除玻璃棒外,还需要___________、________________。
(2)写出硫酸溶解黑色固体的化学方程式:。
(3)为达到资源综合利用的目的,把洗涤滤渣B得到的洗涤液和滤液B合并后,经加热浓缩、________、________ 等操作回收绿矾晶体(FeSO4·7H2O)
(4)在洗涤过程中,用________________________(写试剂的化学式)洗涤滤渣B。
(5)若不考虑生产过程中的损耗,要计算粗铜粉中Cu的含量,需要测定的数据是:最终所得氧化铜的质量和__________________________________________(用文字表示)。
煤能源是我国现阶段主要的能源之一,但煤燃烧排放的SO2会污染环境,某发电厂采用“亚硫酸钠循环法”吸收SO2,其基本过程是:用NaOH溶液在低温下吸收SO2,得到Na2SO3;将生成的Na2SO3溶液继续吸收SO2,得到NaHSO3,将生成的NaHSO3吸收液加热再生,回收释放出的纯SO2气体,并将得到的Na2SO3返回吸收系统。
(1)SO2遇水会形成。
(2)写出下列反应的化学方程式:
①NaOH溶液吸收SO2:;
②NaHSO3吸收液加热再生:。
(3)氢气是未来的绿色能源之一,若你戴上一副能够看清分子、原子等微粒的眼镜,则观察到氢气燃烧过程的现象是:
。
元宵节是我国的重要传统节日,“接汉疑星落,依楼似月悬。”是唐代著名诗人卢照邻对其盛况的写照,我国许多地方至今仍保留着燃灯放焰、共吃元宵的风俗。
(1)某红焰烟花的配方中包括硫、木炭粉、硝酸锶【Sr(NO3)2】等。
①硝酸锶中Sr的化合价为:______________________;
②写出硫燃烧的化学方程式:______________________;
(2)燃放孔明灯(如右图)祈福成为了元宵节的新风尚。小新同学想自制孔明灯,为了使它能飞得更高、更远、更安全,选择作为灯罩的材料应质轻且_____________________;选择的燃料应燃烧热值大且______________;
(3)我市已禁止燃放孔明灯,因为孔明灯燃烧时外焰温度高达300多度,一旦飘落到加油站、液化气站、油库等地,孔明灯会_______________________而引发火灾。(填序号)
A.提供可燃物 B.供给氧气 C.使温度达到可燃物的着火点