下列关于各物质的化学用语表达正确的是
A.四氯化碳的电子式: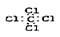 |
B.丙烷分子的比例模型: |
C.环己烷的结构简式: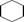 |
D.乙酸的分子式为:CH3COOH |
下列有关生活中的化学,说法不正确的是
| A.食用植物油的主要成分是高级不饱和脂肪酸甘油酯 |
| B.福尔马林可制备标本是利用了使蛋白质变性的性质 |
| C.棉花和蚕丝的主要成分都是纤维素 |
| D.银氨溶液可以用于区分麦芽糖和蔗糖 |
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得: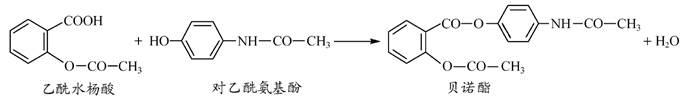
下列有关叙述正确的是
| A.贝诺酯分子式为C17H13NO5 |
| B.可用浓溴水区别乙酰水杨酸和对乙酰氨基酚 |
| C.乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应 |
| D.1 mol贝诺酯与足量NaOH溶液反应,最多消耗4 mol NaOH |
分子式为C10H12O2的有机物,满足以下两个条件:①苯环上有两个取代基,②能与NaHCO3反应生成气体。则满足条件的该有机物的同分异构体有
| A.9种 | B.10种 | C.12种 | D.15种 |
有机物A和B是正处于临床试验阶段的小分子抗癌药物,结构如下图所示,关于有机物A和B的叙述,正确的是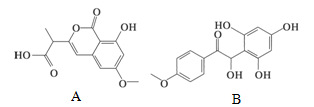
| A.二者都能与Br2发生反应,等物质的量A和B最多消耗的Br2的比例为2: 3 |
| B.有机物A 和B既可以与FeCl3溶液发生显色反应,又可以和NaHCO3 溶液反应 |
| C.1 mol B最多能与6 mol氢气反应 |
| D.等物质的量A和B最多消耗的氢氧化钠质量比为1:1 |