为测定某盐酸的溶质质量分数,取200g样品于烧杯中,将50g碳酸钠溶液分为5等份,分5次加入盛有样品的烧杯中。测出每次反应后溶液的总质量,实验数据如下表:
第一次 |
第二次 |
第三次 |
第四次 |
第五次 |
|
加入Na2CO3溶液的质量 |
10g |
10g |
10g |
10g |
10g |
反应后溶液的质量 |
208.9g |
217.8g |
226.7g |
235.6g |
245.6g |
请根据实验数据计算盐酸的溶质质量分数。
高纯的单晶硅是重要的半导体材料。制备高纯硅的化学方程式为:SiCl4 +2H2高温 Si+ 4HCl。请计算要获得56g硅(Si),至少需要氢气的质量。
某校化学兴趣小组同学用一瓶含有少量氯化钠的硫酸钠固体样品,进行如下图所示的实验。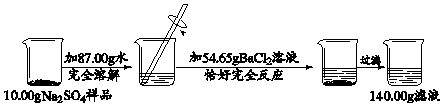
已知:Na2SO4 + BaCl2 = BaSO4↓ + 2NaCl
请根据以上信息,计算反应后所得溶液中溶质的质量分数。
某碱厂的主要产品之一是小苏打(碳酸氢钠),为了测定产品中碳酸氢钠的质量分数(假设该样品中只含氯化钠一种杂质).取样品10.0g逐滴加入稀盐酸,生成CO2气体的质量与滴加稀盐酸的质量关系如下图所示.(有关反应:NaHCO3+HCl=NaCl+H2O+CO2↑)
求:(1)样品中碳酸氢钠的质量分数.
(2)恰好完全反应时,所得溶液中溶质的质量分数.
将铜和氧化铜固体混合物粉末11.2g放入烧杯中,当加入稀硫酸100 g时,氧化铜与硫酸恰好完全反应.过滤后所得溶液的质量为108g,(不考虑过滤过程中溶液的质量损失).
(1)混合物中铜元素的质量分数为 (计算结果保留到0.1%)
(2)求稀硫酸中H2SO4的质量分数.(写出计算过程)
工业上用煅烧石灰石(主要成分为CaCO3)制取生石灰,其生产流程图如下:
(1)某工厂用12t含碳酸钙为75%的石灰石,其中所含碳酸钙的质量是 t.
(2)上述石灰石理论上可以制得生石灰多少t?(写出计算过程)