2021年3月,中央财经会议明确把碳达峰、碳中和纳入生态文明建设整体布局,争取在2060年前实现碳中和。“碳中和”是指在一定时间内产生的二氧化碳排放总量,通过二氧化碳去除手段来抵消掉这部分碳排放,达到“净零排放”的目的。
(1)二氧化碳是引起温室效应的主要气体,根据图甲回答支持这一结论的信息是: 。
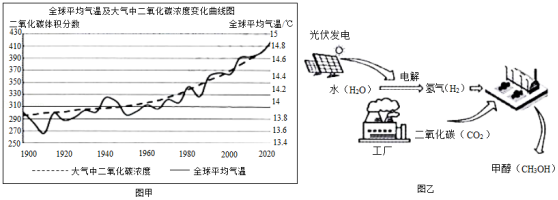
(2)科学家已经研究出多种方式来实现二氧化碳的转化。
①固碳的另一种方法是将收集的二氧化碳和水混合后注入地下玄武岩中,最终与岩石中的矿物质作用形成固态的石头碳酸盐。这种固碳方式属于 变化(选填“物理”或“化学”)。
②我国研发的“液态太阳燃料合成技术”(图乙),甲醇(CH3OH)等液体燃料被形象地称为“液态阳光”。甲醇制取过程中能量转化是:太阳能→电能→ 能。甲醇合成时,若碳元素全部来自于二氧化碳,则制取10吨甲醇需要消耗二氧化碳 吨。
(二氧化碳转化成甲醇的方程式为:CO2+3H2 CH3OH+H2O)
CH3OH+H2O)
课外活动小组的同学们取氯化钠和碳酸钠的混合物34.9克,加入49.5克水中完全溶解,再加入一定量的稀盐酸恰好完全反应,生成二氧化碳的质量为4.4克,此时溶液的溶质质量分数为20%。
求:(1)原混合物中碳酸钠的质量分数;
(2)稀盐酸的溶质质量分数。
某同学取氯酸钾和二氧化锰混合物15.5 g,加热至完全反应得到10.7 g固体,问10.7 g固体中有哪些物质,各有多少克?
化学活动小组欲用溶质质量分数98%的浓硫酸,配制某实验所需的溶质质量分数为19.6%的稀硫酸,并测定所配制的稀硫酸是否符合实验要求。
(1)配制稀硫酸:
①计算配制200g稀硫酸需浓硫酸 g。
②正确的配制方法是 。
(2)测定所配制稀硫酸的溶质质量分数:取50g所配制的稀硫酸于烧杯中,滴入几滴石蕊试液后,逐滴滴入溶质质量分数为10%的NaOH溶液,当消耗77.6gNaOH溶液时恰好完全反应。
①实验中观察到 ,说明恰好完全反应。
②计算所配制的稀硫酸的溶质质量分数(请写出计算步骤,得数保留到0.1%)。
已知CuSO4溶液对过氧化氢的分解也有催化作用。取溶质质量分数为8.5%的过氧化氢溶液20g倒入小烧杯中,向其中加入溶质质量为0.75g 的CuSO4溶液10.8g,使过氧化氢完全分解。试计算:
(1)产生氧气的质量;
(2)反应后所得溶液中CuSO4的质量分数。
7g石灰石样品与52.7g稀盐酸恰好完全反应后(样品中的杂质既难溶于水,又不与稀盐酸反应),生成了2.2g二氧化碳。(溶解在水中的二氧化碳忽略不计)计算:该石灰石样品中碳酸钙的质量分数。