某兴趣小组通过以下实验探究气体的制取方法和性质。
已知:白色的无水硫酸铜与水反应生成蓝色的硫酸铜晶体;浓硫酸具有吸水性。
(1)小清同学整理部分装置(如图1),请你帮他完成下表:
实验室制取气体 |
反应原理(写化学方程式) |
发生装置(填字母) |
收集装置(填字母) |
二氧化碳(干燥) |
|
|
|

(2)小华同学设计的实验装置(如图2),既可用于制取气体,又可用于验证物质性质。
Ⅰ.当打开K1、关闭K2时,利用①、②装置可直接进行的实验是 (填字母)。
A.过氧化氢溶液和二氧化锰混合制取氧气
B.锌与稀硫酸反应制取氢气
Ⅱ.实验Ⅰ中制得的气体不纯。小明同学认为杂质可能为水蒸气,这是科学探究中的 。
A.提出问题
B.做出假设
C.进行实验
D.获得结论
打开K2、关闭K1,利用①、③装置来验证产生的气体中含水蒸气,此时仪器甲中盛放的物质是 ,可以观察到的现象是 。
Ⅲ.仪器甲具有多种用途,小亮同学利用它制氧气并验证氧气性质:

实验过程中观察到的现象为 。对反应后的固体残渣(二氧化锰)进行回收,你认为需要用到的一种操作是 。
请阅读下面的文章,并据此回答问题:
科学家在研究大气中
的浓度变化会对地球的平均气温造成什么影响的问题时,采用的研究途径之一是:研究古气候大气中
的浓度变化和当时大气平均温度的变化关系.
(1)有种方法是测量浅海贝类化石中硼、钙元素含量的比例.因为这个比例高低和这些贝类生长时的海水酸碱度有关,而海水酸碱度又和大气中
的浓度有关.将得到的有关数据和通过其它研究途径得到的同时期大气平均温度对比,即可得到同时期大气平均温度与大气中
的浓度的对应关系.海水酸碱度和大气中
的浓度有关的科学原理是.
请在下列坐标图中,标出坐标轴的含义,并大致表示大气中
的浓度对海水酸碱度(用海水pH表示,海水略呈弱碱性)的影响关系.
(2)科学家也通过另外途径研究古气候时
的浓度变化与当时大气平均温度的关系.
如比较古代植物叶片化石及近现代植物标本,发现很多地区较多同种近现代植物叶片单位面积上气孔数目减少.从植物对环境的适应性考虑,造成这种变化的可能原因是:、(请写出两种).
(3)在生物圈中,你认为当前影响大气中
浓度变化的主要直接因素是:、(请写出两点).
亚硫酸盐的一些性质和碳酸盐的性质类似,如:
(亚硫酸钠)溶液呈碱性,
(亚硫酸钡)是白色难溶于水的固体.工业上常用
来吸收
气体.现有吸收
一段时间后的
样品,请选用下列试剂:盐酸、稀硫酸、蒸馏水、
溶液、
溶液[已知
溶液呈中性〕、
试纸、石蕊指示剂,仪器自选,设计一个简单的实验判断该样品
是否反应完全,请完成下列实验步骤;
(1)取少量吸收
一段时间后的
样品,用适量蒸馏水完全溶解;
(2)用试管取少量该样品溶液;
(3)往试管中逐滴加入,到时,停止加入;
(4)后续实验的操作是:,若观察到,则
已完全反应.
某同学做了如下实验(1)取甲、乙两试管,分别加人1%淀粉溶液各4毫升.(2)甲试管内加入2毫升唾液,乙试管内加入2毫升蒸馏水.(3)同时将两试管置于37℃的温水中恒温10分钟后取出,分别滴加1滴碘液.(4)观察结果.请回答下列问题:
(1)该实验的目的是
(2)请设计一张实验记录表,将实验步骤及正确操作后观察到的实验结果填入表中.
(3)有同学认为设计上述实验时,应确保甲、乙两支试管中的pH相同,但不必考虑pH大小.你认为这种说法是否正确?,说出理由.
某实验小组利用废硫酸液制备
并研究
加热分解的产物.
(一)
的制备
(1)将
研成粉末的目的是.
(2)上述流程中可循环使用的物质有
和(填写化学式).
(3)反应Ⅲ中相关物质的溶解度如下表.你认为反应Ⅲ在常温下能实现的原因是.
| 物质 |
|
M |
||
| 溶解度/g(25℃) |
34.0 |
11.1 |
37.2 |
19.5 |
(4)不用水而用饱和
溶液洗涤反应Ⅲ所得晶体的目的是;为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入(选填序号,下同),振荡、静置,再向上层清液中滴加,观察现象即可判断.
a.
溶液 b.过量的
溶液 c.过量的
溶液
(二)研究
加热分解的产物.
(5)分离所得的
含有
,可用盐酸除去,该的化学反应方程式.
(6)为了测定
和
的质量比x:y,实验小组利用如图所示的装置(夹持仪器省略)进行实验.
①实验前首先要,再装入样品.装置A的作用是.
②已知
在160℃生成
,1350℃时
开始分解;
在900℃时分解完全.现控制B装置温度900℃进行实验并采集了如下数据:
a.反应前玻璃管与样品的质量m1g b.反应后玻璃管中固体的质量为m2g
c.装置C实验后增重m3g d.装置D实验后增重m4g
某同学选用b、d或c、d数据组合求出x:y的值,若无装置E,则实验测定结果将(填"偏大"、"偏小"或"无影响").你认为还可选用上述的(选填序号)两个数据组合也可求出x:y的值.
(7)
受热会逐步失去结晶水.取纯净
固体3.44g,放在(5)的实验装置B中进行加热,测定固体质量随温度的变化情况如图所示.①G点固体的化学式是.
②将T2~1400℃温度段加热固体所产生的气体通入酸性
溶液中,溶液褪色,则H~I段发生反应的化学方程式为.
请结合下图回答问题: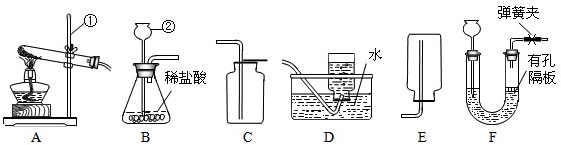
(1)标号①②的仪器名称:①,②.
(2)实验室选用
装置制取
,气体收集完毕时,应先(填"从水中取出导气管"或"熄灭酒精灯").
(3)实验室可用
固体和熟石灰混合加热制取
,应选择发生装置为(选填序号).
(4)选择发生装置
和收集装置(选填序号)可以用于实验室制取
,若将发生装置由
改为
,其优点是.
①为了得到纯净、干燥的
,除杂装置(如图)的导管按气流方向连接顺序是(选填字母);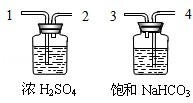
a.1→2→4→3 b.2→1→3→4
c.4→3→1→2 d.3→4→2→1
用化学反应方程式表示饱和
溶液的作用.
②写出用澄清石灰水检验
的化学反应方程式.