电池是一种以海水为电解质溶液的水激活电池.下列叙述错误的是( )
A. 负极反应式为Mg﹣2e ﹣=Mg 2+
B. 正极反应式为Ag ++e ﹣=Ag
C. 电池放电时Cl ﹣由正极向负极迁移
D. 负极会发生副反应Mg+2H 2O=Mg(OH) 2+H 2↑
在C(s)+CO2(g) 2CO(g)反应中可使反应速率增大的措施是
2CO(g)反应中可使反应速率增大的措施是
①缩小容器的体积 ②增加碳的量 ③通入CO2
④恒压下充入N2 ⑤恒容下充入N2 ⑥通入CO
| A.①③⑤ | B.②④⑥ | C.①③⑥ | D.③⑤⑥ |
关于锌、铜和稀H2SO4构成的原电池的下列说法中正确的是
| A.锌溶解的速率比锌直接与同浓度硫酸反应快 |
| B.电子从铜片经导线流向锌片 |
| C.负极的反应式为2H++2e-===H2↑ |
| D.反应一段时间后,溶液的pH降低 |
中国纳米技术的研究能力已跻身于世界的前列。例如曾作为我国十大科技成果之一的就是合成一种—维纳米的材料,化学式为RN。已知该化合物里与氮离子结合的Rn+核外有28个电子。则R位于元素周期表的
| A.第三周期VA族 | B.第四周期IIIA族 |
| C.第四周期VA族 | D.第五周期IIIA族 |
下列反应中不属于加成反应的是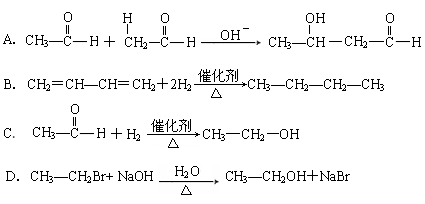
“绿色化学”要求在化工合成过程中,目标产物对反应物的原子利用率达到100%,下列反应类型最符合这一要求的是
| A.取代反应 | B.加成反应 | C.氧化反应 | D.置换反应 |