和 都是锂离子电池的电极材料,可利用钛铁矿(主要成分为 , 还含有少量MgO、 等杂质)来制备,工艺流程如下:

回答下列问题:
(1)"酸浸"实验中,铁的浸出率结果如下图所示.由图可知,当铁的净出率为70%时,所采用的实验条件为________.

(2)"酸浸"后,钛主要以 形式存在,写出相应反应的离子方程式________.
(3) 沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
温度/℃ |
30 |
35 |
40 |
45 |
50 |
92 |
95 |
97 |
93 |
88 |
分析40℃时 转化率最高的原因________.
(4) 中Ti的化合价为+4,其中过氧键的数目为________.
(5)若"滤液②"中 , 加入双氧水和磷酸(设溶液体积增加1倍),使 恰好沉淀完全即溶液中 , 此时是否有 沉淀生成?________(列式计算). 、 的分别为 、
(6)写出"高温煅烧②"中由FePO 4制备 的化学方程式________.
生活中有很多现象都蕴藏着化学秘密,如果你是一个细心的人,就一定会发现很多有趣的事。
(1)煤气灯曾是十八世纪的主要照明工具,但有一个奇怪的事引起了不少人的注意,那就是在有些煤气灯的附近,树叶比其他树要早落好长时间,但这个问题一直到1901年才由俄国的植物学家奈刘波夫证实是煤气灯产生的一种气体在作怪,你认为这种气体可能是________。(填物质名称)
(2)为了证明你的判断,下列是一位同学做的实验及其装置:
如果实验时无水硫酸铜变蓝色,澄清的石灰水变浑浊;你认为通过以上实验可以得出的结论是________________________________________________。
(3)若要进一步得出该分子的组成,另一个同学设计的实验及其装置: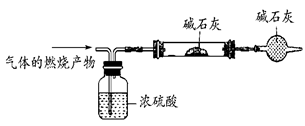
要达到实验的目的,需要下列哪些数据________(填编号)。
①此气体的质量 ②浓硫酸的增重 ③硬质玻璃管的增重
④干燥管的增重 ⑤此气体的体积(标准状况下)
(4)将这种气体在高温高压条件下与苯甲醛按一定比例混合,结果发现苯甲醛的质量和性质都没有发生变化,且还得到了一种白色固体。试推测苯甲醛的作用是________。得到的白色固体是________,发生的反应是___________(填反应类型)。
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反
应速率的因素。
甲同学研究的实验报告如下表:
| 实验步骤 |
现象 |
结论 |
| ①分别取等体积的2 mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg。 |
反应快慢: Mg>Fe>Cu |
反应物的性质越活泼,反应速率越快。 |
(1)该同学的实验目的是________________________________;
要得出正确的实验结论,还需控制的实验条件是________。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用下图装置进行定量实验。完成该实验应选用的实验药品是______;应该测定的实验数据是____________________________。
(3)在使用铁与稀硫酸反应制氢气时,实验室里选择粗铁比纯铁效果更好,原因是:。
该小组同学设计了甲、乙两套实验装置,对甲酸与甲醇进行了酯化反应的研究:
(1)装置乙中长导管的作用是。
(2)甲酸和甲醇(CH318OH)进行酯化反应的化学方程式。
(3)甲装置还是乙装置好?,其原因是。
(4)实验过程中选用的药品及试剂有:浓H2SO4、甲醇、甲酸还有、两种必备用品。
(5)某同学用装有饱和氢氧化钠的三颈瓶接收甲酸甲酯,几乎没有收集到产物,请给予合理的解释:。
中和热的测定实验的关键是要比较准确地配制一定的物质的量浓度的溶液,在实验过程中要尽量避免热量的散失,要求比较准确地测量出反应前后溶液温度的变化。回答下列问题: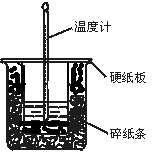
(1)从实验装置上看,图中尚缺少的一种玻璃用品是。
(2)在大小烧杯之间填满碎泡沫(或纸条)其作用是____________________;大烧杯上如不盖硬纸板,求得的中和热数值(填“偏大、偏小、无影响”)
(3)做一次完整的中和热实验,温度计需要使用______ 次;
(4)该实验常用0.50 mol·L-1 HCl和0.55 mol·L-1的NaOH溶液各50 mL。若上述HCl、NaOH溶液的密度都近似为1 g/cm3,中和后生成的溶液的比热容C =" 4.18" J/(g·℃),反应后温度升高了△t, 则生成1mol水时的反应热ΔH="___________" kJ/mol(填表达式)。
(5)如果用50mL0.50mol/L醋酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等、不相等”),简述理由。
已知下列数据:
下图为实验室制取乙酸乙酯的装置图。
(1)当饱和碳酸钠溶液上方收集到较多液体时,停止加热,取下小试管B,充分振荡,静置。振荡前后的实验现象_________(填选项)。
| A.上层液体变薄 | B.下层液体红色变浅或变为无色 |
| C.有气体产生 | D.有果香味 |
(2)为分离乙酸乙酯、乙醇、乙酸的混合物,可按下列步骤进行分离: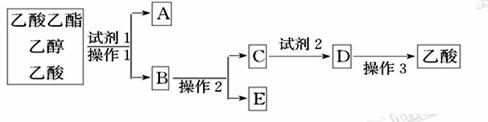
①试剂1最好选用___________;
②操作1是_____,所用的主要仪器名称是________;
③试剂2最好选用___________;
④操作2是___________;
⑤操作3中温度计水银球的位置应为如下图中______(填a、b、c、d)所示,在该操作中,除蒸馏烧瓶、温度计外,还需要的玻璃仪器有_______、_______、_______、______,收集乙酸的适宜温度是___________。