催化重整不仅可以得到合成气(CO和
)。还对温室气体的减排具有重要意义。回答下列问题:
(1) 催化重整反应为: 。
已知:
该催化重整反应的 ________ 。有利于提高 平衡转化率的条件是________(填标号)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
某温度下,在体积为2L的容器中加入 以及催化剂进行重整反应。达到平衡时 的转化率是50%,其平衡常数为________ 。
(2)反中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
积碳反应
|
消碳反应
|
||
|
75 |
172 |
|
活化能/ |
催化剂X |
33 |
91 |
催化剂Y |
43 |
72 |
|
①由上表判断,催化剂X________Y(填"优于或劣于"),理由是________.在反应进料气组成,压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的变化关系如右图所示,升高温度时,下列关于积碳反应,消碳反应的平衡常数(K)和速率(v)的叙述正确的是________(填标号)

| A. | 、 均增加 |
| B. | 减小、 增加 |
| C. | 减小、 增加 |
| D. | 增加的倍数比 增加的倍数大 |
②在一定温度下,测得某催化剂上沉积碳的生成速率方程为 (k为速率常数)。在 一定时,不同 下积碳量随时间的变化趋势如右图所示,则 、 、 从大到小的顺序为________

以硅藻土为载体的五氧化二钒( )是接触法生产硫酸的催化剂.从废钒催化剂中回收 既避免污染环境又有利于资源综合利用.废钒催化剂的主要成分为:
|
物质 |
|
|
|
|
|
|
|
质量分数/% |
2.2~2.9 |
2.8~3.1 |
22~28 |
60~65 |
1~2 |
<1 |
以下是一种废钒催化剂回收工艺路线:

回答下列问题:
(1)"酸浸"时 转化为 , 反应的离子方程式为________,同时 转成 . "废渣1"的主要成分是________.
(2)"氧化"中欲使 的 变为 , 则需要氧化剂 至少为________mol.
(3)"中和"作用之一是使钒以 形式存在于溶液中."废渣2"中含有________.
(4)"离子交换"和"洗脱"可简单表示为: (以ROH为强碱性阴离子交换树脂).为了提高洗脱效率,淋洗液应该呈________性(填"酸""碱""中").
(5)"流出液"中阳离子最多的是________.
(6)"沉钒"得到偏钒酸铵( )沉淀,写出"煅烧"中发生反应的化学方程式________.
卤沙唑仑 是一种抗失眠药物,在医药工业中的一种合成方法如图:

已知:(ⅰ)  +
+ 

 +HCl
+HCl
(ⅱ)  +
+ 

 +H 2O
+H 2O
回答下列问题:
(1) 的化学名称是 。
(2)写出反应③的化学方程式 。
(3) 具有的官能团名称是 。(不考虑苯环)
(4)反应④中, 的结构简式为 。
(5)反应⑤的反应类型是 。
(6) 的同分异构体中,含有苯环并能发生银镜反应的化合物共有 种。
(7)写出 的结构简式 。
过渡金属元素铬 是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)对于基态 原子,下列叙述正确的是 (填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为
B. 电子能量较高,总是在比 电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。 中提供电子对形成配位键的原子是 ,中心离子的配位数为 。
(3) 中配体分子 、 以及分子 的空间结构和相应的键角如图所示。

中 的杂化类型是 。 的沸点比 的 ,原因是 。 的键角小于 的,分析原因 。
(4)在金属材料中添加 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。 具有体心四方结构,如图所示。处于顶角位置的是 原子。设 和 原子半径分别为 和 ,则金属原子空间占有率为 %(列出计算表达式)。

一氯化碘 是一种卤素互化物,具有强氧化性,可与金属直接反应,也可用作有机合成中的碘化剂。回答下列问题:
(1)历史上海藻提碘中得到一种红棕色液体,由于性质相似,Liebig误认为是 ,从而错过了一种新元素的发现。该元素是 。
(2)氯铂酸钡 固体加热时部分分解为 、Pt和 , 时平衡常数 。在一硬质玻璃烧瓶中加入过量 ,抽真空后,通过一支管通入碘蒸气(然后将支管封闭)。在 ,碘蒸气初始压强为 。 平衡时,测得烧瓶中压强为 ,则 ,反应 的平衡常数 (列出计算式即可)。
(3)McMorris 测定和计算了在 范围内下列反应的平衡常数 :
得到 和 均为线性关系,如图所示:

①由图可知, 分解为 和 反应的 (填"大于"或"小于")。
②反应 的 (用 表示);该反应的 (填"大于"或"小于"),写出推理过程 。
(4)Kistiakowsky曾研究了 光化学分解反应,在一定频率(v)光的照射下机理为:
其中 表示一个光子能量, 表示 的激发态。可知,分解 的 需要吸收 的光子。
维生素E是一种人体必需的脂溶性维生素,现已广泛应用于医药、营养品、化妆品等。天然的维生素E由多种生育酚组成,其中α﹣生育酚(化合物E)含量最高,生理活性也最高。下面是化合物E的一种合成路线,其中部分反应略去。

已知以下信息:
a) 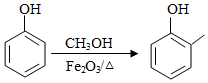
b) 
c) 
回答下列问题:
(1)A的化学名称为 。
(2)B的结构简式为 。
(3)反应物C含有三个甲基,其结构简式为 。
(4)反应⑤的反应类型为 。
(5)反应⑥的化学方程式为 。
(6)化合物C的同分异构体中能同时满足以下三个条件的有 个 (不考虑立体异构体,填标号)。
(ⅰ)含有两个甲基;(ⅱ) 含有酮羰基(但不含C=C=O); (ⅲ) 不含有环状结构。
(a) 4 (b) 6 (c) 8 (d) 10
其中,含有手性碳(注:连有四个不同的原子或基团的碳)的化合物的结构简式为 。