金属材料的使用与生产、生活和社会发展密切相关。
(1)金属冶炼。利用 与 的反应炼铁,反应的化学方程式为 。
(2)金属材料的使用和保护。
①“贵州桥梁”闻名世界。桥梁建造中使用大量钢材作支架,钢是铁的合金,钢的硬度比纯铁的 (填“大”或“小”)
②铁制品在潮湿的空气里容易生锈,防止铁生锈的措施有 。铁也易被酸腐蚀,写出铁与盐酸反应的化学方程式 ,该反应的基本类型是 。
(3)比较 、 、 的金属活动性。

①将一定量的硫酸铜溶液加入锌粉和铁粉的混合固体中,反应的示意图如图所示,分析可知,实验中发生反应的化学方程式为 ,可得结论: 。
②在上述实验中继续添加一定量硫酸铜溶液,微粒种类和数量的变化情况为 时,可得结论:金属活动性 。
下图有多种功能,如收集气体、洗涤气体、贮存气体等。回答下列问题: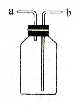
(1)如果用该装置收集二氧化碳(密度比空气大),则二氧化碳从哪端进入集气瓶?
(2)如果用该装置收集氢气(密度比空气小),则氢气从哪端进入集气瓶?
(3)该装置中预先盛满水,将水排出用来贮气,则气体从哪端进入集气瓶?
某同学在实验室里用高锰酸钾加热制取氧气,实验结束后发现试管破裂,请你帮他分析造成试管破裂的可能原因。(写出两条即可)
2014年8月19日,安徽淮南某煤矿发生井下特大瓦斯爆炸事故.瓦斯是煤矿矿井下有害气体的总称,它已成为煤矿事故的“头号杀手”.
(1)瓦斯的主要成分是甲烷.甲烷在空气中完全燃烧的化学方程式为 .
(2)为了防止煤矿的矿井发生瓦斯爆炸事故,下列做法可行的是 (填序号,下同).
A.进矿井前先做灯火实验
B.工人必须戴安全帽才能进入矿井
C.矿井内要加强通风
D.安装瓦斯探头传感器监测瓦斯浓度
(3)矿井下特大瓦斯爆炸事故发生后,专家提出了注入液氮灭火的方案.液氮可用于矿井灭火的原因是 、 (写出两条).
(4)救援过程中,打通“生命之孔”及时向被困人员输送含有下列成分的营养液,该营养液中的主要供能物质是 .
A.水B.葡萄糖
C.维生素 D.氯化钠.
科学家依据蒸汽机原理设计出液氮蒸汽机,即利用液态氮蒸发来驱动机车.
(1)液氮蒸汽机的原理主要依据
| A.氮气做燃料燃烧放热 |
| B.氮气和氢气反应放热 |
| C.氮在空气中约占78% |
| D.氮气沸点为﹣195.8℃,远低于常温 |
(2)请说出液氮蒸汽机的两条优点.
(3)液氮蒸汽机要广泛应用需要克服哪些难题?(答两点)
用微粒的观点解释下列现象:
(1)今年我国要求“公共场所全面禁烟”.非吸烟者往往因别人吸烟而造成被动吸烟,这是因为
(2)夏天钢轨间的缝隙变小: .