在初中化学“金属的性质”中有如下实验:将无锈铁钉浸入 溶液,观察到铁钉表面出现红色物质。研究性学习小组对其展开了进一步探究。

【提出问题】 和 溶液也能发生化学反应吗?
(1)预测 能和 溶液反应,理由是 。
【进行实验】将一端缠绕的铝丝浸入 溶液(如图),观察现象。
(2)铝丝表面未出现红色物质,原因是 。
【实验改进】用砂纸将铝丝表面打磨光亮,将其浸入 溶液,观察现象。
(3)填写实验报告单:
|
序号 |
实验现象 |
结论与解释 |
|
1 |
铝丝表面有少量气泡; 铝丝周围出现蓝绿色物质 |
溶液呈弱酸性,与 反应产生的气体是 ,蓝绿色物质成分待探究 |
|
2 |
24h后,铝丝仍光亮; 48h后,铝丝表面出现少量红色物质 |
红色物质是 ,说明 能和 溶液反应,但反应较慢 |
|
③ |
铝丝周围溶液逐渐变成无色,铝丝以下溶液仍为蓝色; 两层溶液界面清晰 |
反应生成的 为无色; 溶液的密度 (填“>”或“<”) 溶液 |
【深入探究】为研究上述异常现象,同学们查阅了相关资料,继续开展探究。
资料:① 呈蓝绿色,不溶于水;
② 可加快铝丝和其他物质的反应速率。
(4)取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,该反应的化学方程式为 。
(5)欲加快 和 溶液的反应,可加入的物质是 (填一种即可)。
【拓展应用】通过探究,同学们提出了铝制品使用的注意事项。
(6)下列食品不能长时间用铝制炊具盛放的是 (填序号)。
| A. |
食醋 |
| B. |
食用油 |
| C. |
面粉 |
| D. |
咸菜 |
如图所示,为测定空气中氧气的体积含量,将钟罩放入盛水的水槽中,将钟罩内水面以上的容积分为5等份。在燃烧匙内盛有红磷,用酒精灯点燃后,立即插入钟罩内。回答下列问题: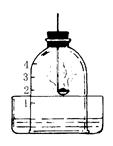
(1)写出红磷燃烧的化学反应的文字表达式:
_________________________________________________。
(2)甲学生用上述装置实验时,发现钟罩内的液面不能升至l处,原因可能是_________________、。(请写出两种)
(3)由该实验还可推知氮气的某些性质,请写出一点:
___________________________________________。
(4)乙同学在实验时用木炭代替了红磷,你认为是否可行?并请说明理由:
。
小明对妈妈杀鱼时从鱼肚内取出的鱼鳔(如图所示)产生了兴趣,他以“探究鱼鳔内气体体积和成分”作为研究性学习的课题,小明通过查阅有关资料获知:这种鱼鳔内氧气约占1/4,其余主要为二氧化碳和氮气,且二氧化碳能溶于水。探究分两步进行: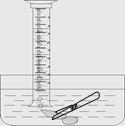
(1)测量鱼鳔内气体体积。小明设计了两种方法:A 用医用注射器抽取鱼鳔内气体,测量其体积;B 在水下刺破鳔,用排水集气法收集鱼鳔内气体并测量其体积(如图所示),你认为测量结果不准确的一种方法是__________,理由是__________________________________。
(2)探究鱼鳔内气体的成分。现有两瓶鱼鳔内的气体,请你帮助小明设计实验进行验证。
| 实验目的 |
实验方法 |
实验现象 |
| 验证鱼鳔内含O2 |
① |
|
| 验证鱼鳔内含CO2 |
② |
过氧化钠是化学中常见的一种药品,它是浅黄色颗粒。易溶于水,能与水发生反应,生成氢氧化钠和过氧化氢,化学方程式:Na2O2+2H2O=2NaOH+H2O2,过氧化氢又能 分解放出氧气。
(1)区分水和过氧化氢的实验方法是:,发生的反应方程式是:_______ ____。
(2)某同学为了证明过氧化钠加入水中生成了氢氧化钠,在生成的溶液中滴加了几滴无色酚酞试液,观察到的现象是溶液先变红后褪为无色,请你对此现象进行探究。
【提出问题】:什么原因导致溶液变红后再褪色的呢?
【猜想与假设】:
猜想1:甲同学“可能是无色酚酞溶液变质导致溶液褪色”;
猜想2:乙同学“可能是生成的过氧化氢使溶液褪色”。
【实验与结论】:
a:甲同学提出的猜想,立即遭到其他同学的反对,因为;
b:为了验证自己的猜想,乙同学设计了以下方案并实验验证:
| 实验步骤 |
实验现象 |
实验结论 |
| 取少量稀氢氧化钠溶液于试管中,滴加1—2滴酚酞试液,变红后 观察现象 |
溶液依然 为红色 |
【讨论交流】:你还能提出不同的猜想吗?如果还能提出新的合理的假设和方案你将获得奖励分4分。(化学试卷总分不超过60分)
猜想3:。
方案3:
| 实验步骤 |
实验现象 |
实验结论 |
小娜同学发现厨房中有两瓶无标签的白色粉末,妈妈告诉她是苏打和小苏打。为了鉴别这两瓶白色粉末,小娜各取了一小包并将它们编号为A、B,然后进行实验探究。
【查阅资料】苏打,学名为碳酸钠, 20℃时溶解度为21.6g,其水溶液呈碱性……
小苏打.学名为碳酸氢钠, 20℃时溶解度为9.8g,其水溶液的碱性比碳酸钠溶液的弱……
【实验探究】根据以上信息及学过的知识,小娜进行了以下的实验: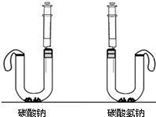
A B
(1)20℃时,将A、B两种物质各6g分别加入到50g蒸馏水中,有白色固体剩余的是;
(2)用pH试纸测得A的溶液pH=10,B的溶液pH=8,则A粉末是; (3)小娜通过计算发现,等质量的碳酸钠与碳酸氢钠与足量的稀盐酸反应,产生的二氧化碳更多,于是设计了下面的实验方案.在U型管中分别加入等质量A、B两种固体,在两支注射器中分别吸入足量稀盐酸,并注入U型管中.请写出碳酸氢钠与稀盐酸反应的化学方程式:。 实验需要观察的现象是。
(3)小娜通过计算发现,等质量的碳酸钠与碳酸氢钠与足量的稀盐酸反应,产生的二氧化碳更多,于是设计了下面的实验方案.在U型管中分别加入等质量A、B两种固体,在两支注射器中分别吸入足量稀盐酸,并注入U型管中.请写出碳酸氢钠与稀盐酸反应的化学方程式:。 实验需要观察的现象是。
【反思提高】(4)小娜想利用上述实验方案进一步探究碳酸钠和碳酸氢钠与盐酸反应的快慢,请从设计方法的角度说明一下是否合理
。
某化学小组对一包干燥的红色粉末组成进行探究。请你参与并回答有关问题。
【教师提醒】它由Cu 、Fe2O3二种固体中的一种或两种组成。
【提出猜想】红色粉末可能的组成有:①只有Cu;
②只有;③是Cu 、Fe2O3的混合物。
【资料获悉】Cu在FeCl3溶液中发生反应:2FeCl3+Cu = 2FeCl2+CuCl2
【实验探究】(1)甲同学取少量红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解。甲同学认为可以排除猜想中的①和③,而乙同学认为只能排除猜想①,你认为的观点正确(填“甲”或“乙”)。
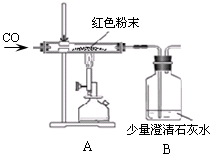
(2)丙同学为进一步确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按右下图在通风橱中进行实验。开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却。反应前后称量相关装置和物质的总质量,其数据如下表:
| 反 应 前 |
反 应 后 |
|
| Ⅰ 组 |
玻璃管和红色粉末的总质量为37.3 g |
玻璃管和固体物质的总质量为36.1 g |
| Ⅱ 组 |
洗气瓶和所盛溶液的总质量为180.0 g |
洗气瓶和瓶中物质 的总质量为183.1 g |
【交流讨论】
(1)在装置A中先通CO气体的作用是。
(2)写出A装置中发生反应的化学方程式;实验中观察到A装置中的现象为。
(3)为了防止溶液倒吸,本实验停止加热前是否需要先断开A和B的连接处?
不需要,。
(答对下面(4)与【反思评价】两小题将奖励4分,但全卷总分不超过60分)
(4)选择组的实验数据计算来确定红色粉末的组成。最终计算结果表明:该红色粉末的组成是猜想中的第组(填序号)。
【反思评价】丁同学指出:从环保角度,上图装置有严重不足之处。你认为应该如何改进?。