下列说法正确的是()
| A. | 晶体中只存在离子键 |
| B. | 含 、 的水都是硬水 |
| C. | 雾是气溶胶,在阳光下可观察到丁达尔效应 |
| D. | 玻璃是氧化物,成分可表示为 |
已知:①2C (s) + O 2(g) = 2CO (g)△H =-221.0 kJ/mol
②C (s) + O 2(g) = CO2 (g) △H =-393.51kJ/mol
计算反应C (s) + CO2 (g) = 2CO (g)的反应热△H为()
| A.+172.51 kJ/mol | B.+283.01 kJ/mol |
| C.-283.01 kJ/mol | D.-504.00 kJ/mol |
氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏 1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol氯气中的化学键消耗的能量为Q2kJ,形成1mol氯化氢中的化学键释放的能量为Q3kJ。下列关系式中,正确的是()
| A.Q1+Q2>Q3 | B.Q1+ Q2<2Q3 | C.Q1+Q2<Q3 | D.Q1+ Q2>2Q3 |
沼气是一种新能源,它的主要成分是CH4 , 当0.5mol CH4完全燃烧生成CO2气体和液态水时,放出445kJ热量,则下列热化学方程式正确的是()
| A.2CH4(g)+4O2(g)=2CO2(g)+4H2O(l); △H=+890kJ/mol |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(l); △H=+890kJ/mol |
| C.CH4(g)+2O2(g)=CO2(g)+2H2O(l); △H=-890kJ/mol |
| D.1/2CH4(g)+O2(g)=1/2CO2(g)+H2O(l); △H=-890kJ/mol |
下列热化学方程式书写正确的是(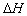 的绝对值均正确)()
的绝对值均正确)()
A.C2H5OH(l)+3O2(g) = 2CO2 (g)+3H2O(g)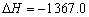 kJ/mol(燃烧热) kJ/mol(燃烧热) |
B.NaOH(aq)+HCl (aq) = NaCl (aq) +H2O(l)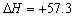 kJ/mol(中和热) kJ/mol(中和热) |
C.S(s)+O2(g) = SO2(g)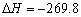 kJ/mol(反应热) kJ/mol(反应热) |
D.Fe+S = FeS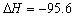 kJ/mol(反应热) kJ/mol(反应热) |
未来氢气将作为新能源的优点的是()
①燃烧时发生氧化反应 ②充分燃烧的产物不污染环境
③氢气是一种再生能源 ④燃烧时放出大量热量
| A.①②③ | B.①②④ | C.①③④ | D.②③④ |