在t℃时,将 a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρg·cm-3,质量分数为ω,其中含NH4+的物质的量为 b moL。下列叙述中正确的是( )
A.溶质的质量分数为ω=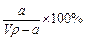 |
B.溶质的物质的量浓度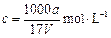 |
C.溶液中c(OH-)= |
| D.上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω |
某有机物A的结构简式为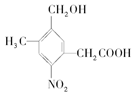 取Na、NaOH和Cu(OH)2分别与等物质的量的A在一定条件下充分反应时,理论上需Na、NaOH和Cu(OH)2三种物质的物质的量之比为
取Na、NaOH和Cu(OH)2分别与等物质的量的A在一定条件下充分反应时,理论上需Na、NaOH和Cu(OH)2三种物质的物质的量之比为
| A.2:2:1 | B.4:2:1 | C.2:1:2 | D.1:1:1 |
下列烷烃在光照下与氯气反应,只生成一种一氯代烃的是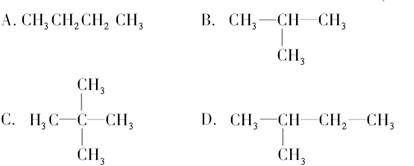
下列叙述正确的是
| A.糖类都有甜味,都易溶于水 |
| B.糖类都能发生银镜反应 |
| C.油脂属酯类,不溶于水,属高分子化合物 |
| D.蛋白质属高分子化合物 |
主链为4个碳原子的己烯共有几种结构
| A.2种 | B.3种 | C.4种 | D.5种 |
苹果醋是一种由苹果发酵而成健康食品.苹果酸(a羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构式为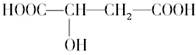 ,下列说法不正确的是
,下列说法不正确的是
| A.苹果酸在一定条件下能发生酯化反应 |
| B.苹果酸在一定条件下能发生催化氧化反应 |
| C.苹果酸在一定条件下能发生消去反应 |
| D.1 mol苹果酸与Na2CO3溶液反应最多消耗3 mol Na2CO3 |