下列关于氯的说法正确的是
A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂 |
B.若35 17Cl、37 17若Cl为不同的核素,有不同的化学性质 |
C.实验室制备Cl2,可用排放和食盐水集气法收集 |
D.1.12LCl2含有1.7NA个质子(NA表示阿伏伽德罗常数) |
已知反应CO(g) + 2H2(g) CH3OH(g)的能量情况如图所示,曲线I和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是
CH3OH(g)的能量情况如图所示,曲线I和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是
| A.该反 应的ΔH=+91kJ·mol-1 |
| B.加入催化剂,该反应的ΔH变小 |
| C.反应物的总能量大于生成物的总能量 |
| D.如果该反应生成液态CH3OH,则ΔH增大 |
下列叙述错误的是
| A.废弃的干电池不能随意丢弃,但可以土埋处理 |
| B.马口铁(镀锡铁)镀层破损后即失去保护作用 |
| C.不能将铁制自来水管与铜制水龙头连接使用 |
| D.电化学腐蚀过程中存在电极反应,产生微电流 |
某同学按图示装置进行实验:A极是铜锌合金,B极为纯铜,溶液为足量的硫酸铜溶液。通电一段时间后,若A极恰好全部溶解,此时B极质量增加5.76g,溶液质量增0.03g,则合金中Cu、Zn原子个数比为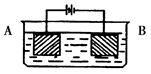
| A.4:1 | B.3:1 | C.2:1 | D.任意比 |
下列实验装置符合实验目的是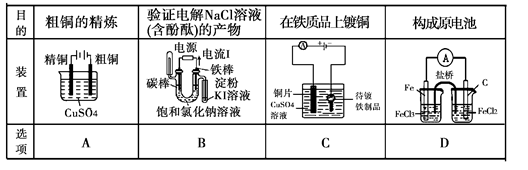
在一容积为2 L的密闭容器中,加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生反应:N2(g)+3H2(g)  2NH3(g) ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示。反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为
2NH3(g) ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示。反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为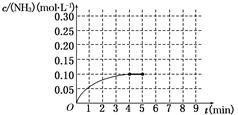
| A.0.20 mol·L-1 | B.0.12 mol·L-1 |
| C.0.10 mol·L-1 | D.0.08 mol·L-1 |