X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为 、 ;
(2)XZ2与YZ2分子的立体结构分别是 和 ,相同条件下两者在水中的溶解度较大的是 (写分子式),理由是 ;
(3)Q的元素符号是 ,它属于第 周期,它的核外电子排布式为 ,在形成化合物时它的最高化合价为 ;
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键 。
火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.8mol液态肼和1.6mol H2O2混合反应,生成氮气和水蒸气,放出513.4kJ的热量(相当于25℃、101 kPa下测得的热量)。
(1)反应的热化学方程式为。
(2)又已知H2O(l)=H2O(g) ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是kJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是。
反应A(g)+B(g)  C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
(1)该反应是____________________反应(填“吸热”、“放热”)。
(2)反应体系中加入催化剂对反应热是否有影响?_______________,原因是_________.
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_________,E2________(填“增大”、“减小”或“不变”)。
可逆反应:aA(g)+ bB(g)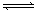 cC(g)+ dD(g);根据图回答:
cC(g)+ dD(g);根据图回答: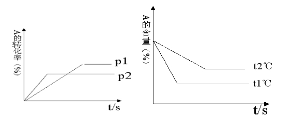
(1)压强 P1比P2(填大或小);
(2)(a +b)比(c +d)(填大或小);
(3)温度t1℃比t2℃(填高或低);(4)正反应为反应。
下图是在其它条件一定时,反应2NO+O2≒2NO2+ Q(Q>0)中NO 的最大转化率与温度的关系曲线。图中坐标有A、B、C、D、E 5点,其中表示未达平衡状态且V正>V逆的点是。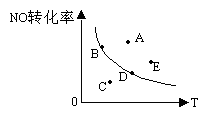
某高温下,金属镁和镍分别在氧气中进行氧化反应时,在金属表面生成氧化薄膜的实验数据记录如下:
| 反应时间t/h |
1 |
4 |
9 |
16 |
25 |
| MgO层厚Y/nm NiO层厚Y'/nm |
0.05a b |
0.2a 2b |
0.45a 3b |
0.80a 4b |
1.25a① 5b② |
①②a和b均为与温度有关的常数。
请回答下列问题:
(1)金属高温氧化腐蚀速率可以用金属氧化膜的生长速率来表示,其理由是_______
________________________。
(2)金属氧化膜的膜厚Y跟时间t所呈现的关系是(填“直线”、“抛物线”、“对数”或“双曲线”等类型):MgO氧化膜的膜厚Y属____型;NiO氧化膜的膜厚Y'属____型。
(3)Mg与Ni比较,哪一种金属具有更良好的耐氧化腐蚀性?答:_________,其理由是_____________________________________________________________。