化学实验中常将溶液或试剂进行酸化,下列酸化处理的措施正确的是( )
| A.检验溶液中是否含有SO32-时,用硝酸酸化后再加BaCl2溶液 |
| B.为提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液酸化 |
| C.检验溶液中是否含有Fe2+时,用硝酸酸化后,加KSCN溶液 |
| D.检验溶液中是否含有SO42-时,用盐酸酸化后,加BaCl2溶液 |
某无色溶液中加入氢氧化铝,氢氧化铝迅速溶解,则该溶液中一定能够大量共存的离子组是
| A.K+、Ba2+、NO3-、Cl- | B.Na+、K+、CO32—、SO42- |
| C.Na+、K+、Fe2+、NO3- | D.Na+、Fe3+、Cl—、SCN— |
某探究小组利用丙酮的溴代反应:
(CH3COCH3+Br2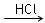 CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系。反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据。分析实验数据所得出的结论不正确的是
CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系。反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据。分析实验数据所得出的结论不正确的是
| 实验 序号 |
初始浓度c/mol??L-1 |
溴颜色消失 所需时间t/s |
||
| CH3COCH3 |
HCl |
Br2 |
||
| ① |
0.80 |
0.20 |
0.0010 |
290 |
| ② |
1.60 |
0.20 |
0.0010 |
145 |
| ③ |
0.80 |
0.40 |
0.0010 |
145 |
| ④ |
0.80 |
0.20 |
0.0020 |
580 |
| A.增大c(CH3COCH3),v(Br2)增大 | B.实验②和③的v(Br2)相等 |
| C.增大c(HCl),v(Br2)增大 | D.增大c(Br2),v(Br2)增大 |
下述做法能改善空气质量的是
| A.以煤等燃料作为主要生活燃料 |
| B.利用太阳能、风能和氢能等能源替代化石能源 |
| C.鼓励私人购买和使用汽车代替公交车 |
| D.限制使用电动车 |
下列描述中,错误的是
| A.往下水道中倾倒硫酸铜溶液,会进一步加快铁制管道的腐蚀 |
| B.镁与稀盐酸反应剧烈,加入醋酸钠晶体可以减慢反应速率 |
| C.电解饱和食盐水制氯气时用铁作阳极 |
| D.电解法精炼粗铜,用纯铜作阴极 |
pH=a的某电解质溶液中,插入两支惰性电极,通直流电一段时间后,溶液的pH<a,则该电解是
| A.NaOH | B.HCl | C.H2SO4 | D.Na2SO4 |