太湖、巢湖、滇池是我国重点治理的三大湖,三大湖受到严重的富营养化污染,藻类疯狂繁殖,破坏了生态平衡,影响了人民的健康,必须迅速进行治理。请回答:
(1)藻类的狂长,说明水中哪些元素超标? 这些元素从哪里引入的?
(2)您认为引起藻类大量繁殖最主要的是哪一种元素? 以什么形态出现? 请你设计一个测定此元素的方法。
(3)水质污染程度的重要标志之一为BOD(生物化学耗氧量),它是指由于水中微生物的繁殖或呼吸作用,或水中有机物分解时所消耗的溶解氧的量,单位为mgO2/L。现有巢湖沿岸某电镀厂,不遵守环境法规,每周向湖中排放一次含氰废水,使近岸湖水含CN-的浓度为7.5×10-5mol/L,CN-与O2作用生成CO2、N2等。试问此电镀厂每排放一次废水将使近岸湖水的BOD增大多少?
(4)水质污染程度的另一重要指标为COD(化学耗氧量),它是指水中还原性物质(有机的和无机的),在规定条件下被氧化时,1L水样所消耗的氧的毫克数。测定COD通常有KMnO4法、K2Cr2C7法等。酸性KMnO4法:KMnO4在酸性溶液中经沸水浴加热,将发生:
2KMnO4+3H2SO4==K2SO4+2MnSO4+3H2O+5[O]。
①若为0.01000mol/L KMnO4溶液,则1.00mL相当于 mgO2;
②若巢湖水样100mL,加入1:2 H2SO410mL,AgSO41g,混匀后,又加10mL 0.01000mol/L KMnO4溶液,在沸水中加热30min,取出加入10mL 0.02500mol/L Na2C2O4溶液,立即用0.01000mol/L KMnO4滴至微红色在15秒内不变色为终点,耗KMnO4液7.00mL,求巢湖水样的COD为多少?
⑴第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为 ▲。在GaN晶体中,与同一个Ga原子相连的N原子构成的空间构型为 ▲。在四大晶体类型中,GaN属于 ▲晶体。
⑵铜、铁元素能形成多种配合物。微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有 ▲的原子或离子
⑶CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题: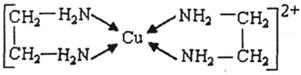
① H、N、O三种元素的电负性由大到小的顺序是 ▲。
②SO2分子的空间构型为 ▲ 。与SnCl4互为等电子体的一种离子的化学式为 ▲
③乙二胺分子中氮原子轨道的杂化类型为 ▲。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是 ▲。
④⑶中所形成的配离子中含有的化学键类型有 ▲。
a.配位键 b.极性键 c.离子键 d.非极性键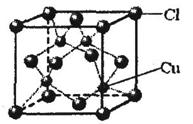
⑤CuCl的晶胞结构如上图所示,其中Cl原子的配位数为 ▲。
(10分)工业上常用废铁屑溶于一定浓度的硫酸溶液制备绿矾( FeSO4·7H2O )。
(1)若用98% 1.84 g/cm3的浓硫酸配制生产用28%的硫酸溶液,则浓硫酸与水的体积比约为1: ▲。
(2)为测定某久置于空气的绿矾样品中Fe2+的氧化率,某同学设计如下实验:取一定量的样品溶于足量的稀硫酸中,然后加入5.00 g铁粉充分反应,收集到224 mL(标准状况)气体,剩余固体质量为3.88 g,测得反应后的溶液中Fe2+的物质的量为0.14 mol(不含Fe3+)。则该样品中Fe2+离子的氧化率为 ▲。
(3)硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](俗称莫尔盐),较绿矾稳定,在氧化还原滴定分析中常用来配制Fe2+的标准溶液。现取0.4 g Cu2S和CuS的混合物在酸性溶液中用40 mL 0.150 mol/L KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与V mL 0.2 mol/L (NH4)2Fe(SO4)2溶液完全反应。已知:MnO4-+Fe2++H+——Mn2++Fe3++H2O(未配平)
①V的取值范围为▲;
②若V=35,试计算混合物中CuS的质量分数。
苯佐卡因是一种医用麻醉药品,学名对氨基苯甲酸乙酯。用芳香烃A为原料合成苯佐卡因E的路线如下:
请回答:
⑴写出结构简式 B ▲C ▲。
⑵写出反应类型① ▲②▲。
⑶化合物D经聚合反应可制得高分子纤维,广泛用于通讯、导弹、宇航等领域。写出该聚合反应的化学方程式: ▲。
⑷下列化合物中能与E发生化学反应的是 ▲。
a. HCl b. NaCl c. Na2CO3 d. NaOH
⑸除 、
、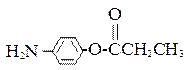 、
、 外,符合下列条件的化合物E的同分异构体有 ▲种。
外,符合下列条件的化合物E的同分异构体有 ▲种。
i. 为1,4—二取代苯,其中苯环上的一个取代基是氨基;
ii. 分子中含 结构的基团
结构的基团
近年我国汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物。
⑴汽车内燃机工作时引起反应:N2(g)+O2(g) 2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则T ℃时该反应的平衡常数
2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则T ℃时该反应的平衡常数
K= ▲。(计算结果保留小数点后两位数字)
⑵一定量的NO发生分解的过程中,NO的转化率随时间变化的曲线如下图所示。(已知:T1<T2)
①反应 2NO(g)  N2(g)+O2(g)为(填“吸热”或“放热”) ▲反应。
N2(g)+O2(g)为(填“吸热”或“放热”) ▲反应。
②一定温度下,能够说明反应 2NO(g)  N2(g)+O2(g) 已达到平衡的是(填序号)▲ 。
N2(g)+O2(g) 已达到平衡的是(填序号)▲ 。
a.容器内的压强不发生变化 b.NO分解的速率和NO生成的速率相等
c.NO、N2、O2的浓度保持不变 d.单位时间内分解4 mol NO,同时生成2 mol N2
⑶①当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染。
已知:CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g)△H1=-574 kJ·mol-1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g)△H2
CH4(g)+2NO2(g) = N2(g)+CO2(g)+2H2O(g)△H3=-867 kJ·mol-1
△H2= ▲。
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NOx)转化为无毒气体,该反应的化学方程式为 ▲。
重铬酸钠(Na2Cr2O7)广泛用于合成颜料、媒染剂等,以铬铁矿(主要成分为Cr2O3,还有FeO、Al2O3、SiO2等杂质)为原料制取重铬酸钠的流程图如下: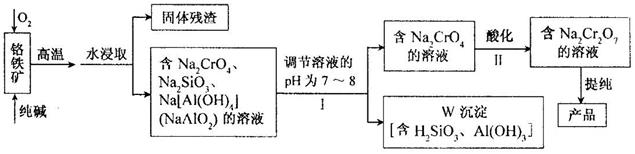
请回答下列问题。
⑴铬铁矿中的Cr2O3与纯碱、O2在高温下反应的化学方程式为 ▲。
⑵若Ⅰ中只用一种试剂调节溶液的pH,应选用 ▲(填标号)。
A.稀硫酸 B.氧化钠固体 C.氢氧化钾溶液
⑶Ⅰ中,调节溶液pH后,如果溶液的pH过小,可能导致W沉淀部分溶解,原因是:
▲。(用离子方程式表示)。
⑷Ⅱ中,Na2CrO4转化为Na2Cr2O7的离子反应如下:
2CrO42-(黄色)+2H+ Cr2O72-(橙红色)+H2O
Cr2O72-(橙红色)+H2O
①该反应 ▲(填“是”或“不是”)氧化还原反应。
②若往Na2Cr2O7溶液(橙红色)中加入足量NaOH固体,溶液 ▲ (填标号)。
A.变黄色 B.颜色不变 C.橙红色变深
③已知:25℃,Ag2CrO4的Ksp=1.12×10-12,Ag2Cr2O7的Ksp=2×10-7。25℃,往Na2Cr2O7溶液中加入AgNO3溶液,最终只生成一种砖红色沉淀,该沉淀的化学式是 ▲。