碳化硅(SiC)的一种晶体具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的。在下列三种晶体①金刚石、②晶体硅、③碳化硅中,它们的熔点从高到低的顺序是 ( )
| A.①③② |
B.②③① |
| C.③①② |
D.②①③ |
| |
|
某温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g) 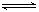 2C(g)达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则()
2C(g)达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则()
A.平衡不移动
B.再达平衡时,n(A)∶n(B)∶n(C)仍为2∶2∶1
C.再达平衡时,C的体积分数增大
D.再达平衡时,正反应速率增大,逆反应速率减小
现有反应:CO(g)+H2O(g) 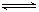 CO2(g)+H2(g)ΔH=-43kJ/mol,在850℃时,K=1,今在某密闭容器中充入1.0molCO、3.0molH2O、1.0molCO2、xmolH2,下列说法不正确的是()
CO2(g)+H2(g)ΔH=-43kJ/mol,在850℃时,K=1,今在某密闭容器中充入1.0molCO、3.0molH2O、1.0molCO2、xmolH2,下列说法不正确的是()
A. ,该反应的平衡常数 ,该反应的平衡常数 |
B. 达到平衡时,通入CO,CO转化率将增大 达到平衡时,通入CO,CO转化率将增大 |
C. 时,若 时,若 ,则起始时平衡向逆反应方向移动 ,则起始时平衡向逆反应方向移动 |
D. 时,若要使上述反应开始时向正反应方向进行,则 时,若要使上述反应开始时向正反应方向进行,则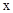 应满足 应满足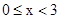 |
某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g) 2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是()
2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是()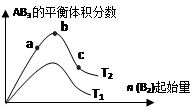
| A.反应速率a>b>c |
| B.达到平衡时,AB3的物质的量大小为:b > c > a |
| C.若T2>T1,则正反应一定是吸热反应 |
| D.达到平衡时A2的转化率大小为:b>a>c |
对于可逆反应 2AB3(g)  A2(g) + 3B2(g) (正反应吸热)下列图像正确的是()
A2(g) + 3B2(g) (正反应吸热)下列图像正确的是()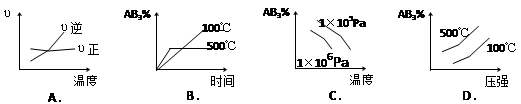
一定条件下,某容积不变的密闭容器内存在下列平衡:2HI(g) H2(g)+I2(g);则下列有关说法正确的是()
H2(g)+I2(g);则下列有关说法正确的是()
| A.如仅仅改变浓度这一条件,使得体系颜色加深,则上述平衡在条件改变之后的移动方向无法判断:即可以正移或逆移,还可以不移动 |
| B.如改变体系温度,体系颜色一定发生变化 |
| C.继续充入HI气体,则HI的转化率将减小 |
| D.温度不变时,当体系颜色变浅,则正反应速率和逆反应速率都将减小 |