可用下图装置制取(必要时可加热)、净化、收集的气体是 ( )
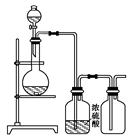 |
| A. | 铜和稀硝酸制一氧化氮 | B. | 氯化钠与浓硫酸制氯化氢 |
| C. | 锌和稀硫酸制氢气 | D. | 硫化亚铁与稀硫酸制硫化氢 |
核外电子是有规律地进行排布的,它们分层排布在K、L、M、N、O……层上,下列叙述正确的是
| A.K层上容纳的电子数只能是2个 | B.K层上容纳的电子数可以超过2个 |
| C.L层上最多只能容纳8个电子 | D.最外 层上容纳的电子数可以超过8个 层上容纳的电子数可以超过8个 |
不能作为元素周期表中元素排列顺序的依据的是
| A.原子的核电荷数 | B.原子的核外电子数 |
C.原子的质子数 |
D.原子的中子数 |
关于元素周期表的下列叙述,错误的是
| A.元素周期表揭示了化学元素间的内在联系,是化学发展史上的重要里程碑之一。 |
| B.在周期表中,把电子层数相同的元素排成一横行,称为一周期 |
| C.元素周期表中,总共有18个纵行,18个族 |
| D.第IA族的元素又称为碱金属元素(除了H),第VIIA族的元素又称为卤族元素 |
下列说法中不正确的是
| A.金属的冶炼原理,就是利用氧化还原反应原理,用还原剂在一定条件下将金属从矿石中还原出来 |
| B.冶炼金属时,必须加入一种物质作为还原剂 |
| C.金属由化合态变为游离态,都是被还原 |
| D.金属单质被发现和应用得越早,其活动性一般较弱 |
下列有关热化学方程式的叙述正确的是
| A.已知C(石墨,s)→C(金刚石,s);△H>0,则金刚石比石墨稳定 |
B.已知C(s)+O2(g) →CO2(g);△H1和C(s)+1/2O2= CO(g);△H2,则△H1>△H2 CO(g);△H2,则△H1>△H2 |
| C.在101KPa时,2 H2 (g)+ O2 (g) ="2" H2O(l);△H =-571.6kJ·mol-1,则2mol液态水分解成2mol氢气和1mol氧气吸收571.6KJ的热量 |
| D.含20.0gNaOH的稀溶液与稀盐酸完全中和时放出28.7kJ的热量,则该反应的热化学方程式为:NaOH(aq)+HCl(aq)="NaCI(aq)+" H2O(l);△H =+57.4 kJ·mol-1 |