下列说法不正确的是( )
| A.电解熔融的氯化钠中铁电极连接电源的负极 |
| B.电解熔融的氯化钠中石墨电极作阳极发生氧化反应 |
| C.可用电解饱和氯化钠溶液来制备金属钠 |
| D.熔融氯化钠的电离是在电流的作用下发生的 |
下图曲线a和b是盐酸与氢氧化钠溶液的相互滴定的滴定曲线,下列叙述正确的是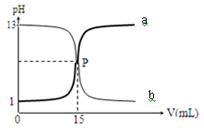
| A.NaOH溶液的浓度为0.1 mol·L-1 |
| B.P点时可能未完全反应,溶液呈可能呈酸性 也可能呈碱性 |
| C.曲线a是盐酸滴定氢氧化钠溶液的测定曲线 |
| D.本实验的指示剂不能用甲基橙,只能用酚酞 |
在某2L恒容密闭容器中充入2 mol X(g)和1 mol Y(g)发生反应:2X(g)+Y(g) 3Z(g)△H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g)△H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是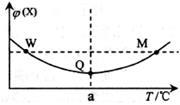
| A.M点时,Y的转化率最大 |
| B.升高温度,平衡常数减小 |
| C.平衡后充入Z达到新平衡时Z的体积分数增大 |
| D.W,M两点Y的正反应速率相等 |
现有阳离子交换膜、阴离子交换膜、石墨电极和如图所示的电解槽。用氯碱工业中的离子交换膜技术原理,可电解Na2SO4溶液生产NaOH溶液和H2SO4溶液。下列说法中正确的是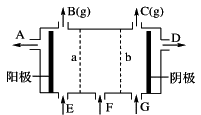
| A.b是阳离子交换膜,允许Na+通过 |
| B.从A口出来的是NaOH溶液 |
| C.阴极反应式为4OH--4e-= 2H2O+O2↑ |
| D.Na2SO4溶液从G口加入 |
硫酸亚锡(SnSO4)是一种重要的能溶于水的硫酸盐,广泛应用于镀锡工业。SnSO4的实验室制备设计路线如下: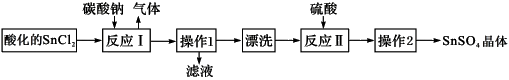
下列有关说法正确的是
| A.SnCl2酸化是为了防止溶解时发生水解 |
| B.反应I中发生的离子反应为:CO32-+2H+=CO2↑+ H2O |
| C.漂洗时,将固体置于烧杯中,加蒸馏水洗涤过滤2-3次 |
| D.操作1为过滤,操作2为盐析 |
光谱研究表明,易溶于水的SO2所形成的溶液中存在着下列平衡: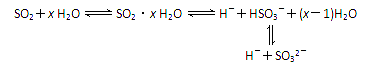
据此,下列判断中正确的是
| A.该溶液中存在着SO2分子 |
| B.该溶液中H+浓度是SO32-浓度的2倍 |
| C.向该溶液中加入足量的酸SO2气体都能放出 |
| D.向该溶液中加入NaOH可得到Na2SO3、NaHSO3和NaOH的混合溶液 |