t℃时,水的离子积为Kw。在该温度下,混合可溶性的一元酸HA和一元碱BOH的溶液,下列有关混合液的各种关系中,可确认混合液呈中性的是
| A.pH=7 | B.C(A-)>c(B+) |
C.C(OH-)= |
D.C(H+)- C(OH-)=C (A-)- C(B+) |
据科学家预测,月球的土壤中吸附着数百万吨的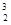 He,每百吨
He,每百吨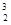 He核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以
He核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以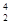 He的形式存在。下列说法正确的是( )。
He的形式存在。下列说法正确的是( )。
A.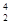 He原子核内含有4个质子 He原子核内含有4个质子 |
B.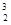 He和 He和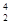 He互为同位素 He互为同位素 |
C.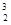 He原子核内含有3个中子 He原子核内含有3个中子 |
D.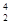 He的最外层电子数为2,所以 He的最外层电子数为2,所以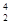 He具有较强的金属性 He具有较强的金属性 |
有aXn+和bYm-两种元素的简单离子,若它们的电子层结构相同,则下列关系正确的是( )。
| A.b-a=n+m | B.a-b=n-m |
| C.核电荷数Y<X | D.质子数Y>X |
1919年,科学家第一次实现了人类多年的梦想——人工转变元素。这个核反应如下: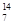 N+
N+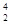 He―→
He―→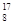 O+
O+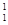 H,下列叙述正确的是( )。
H,下列叙述正确的是( )。
A.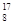 O原子核内有9个质子 O原子核内有9个质子 |
B.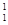 H原子核内有1个中子 H原子核内有1个中子 |
| C.O2和O3互为同位素 |
| D.通常情况下,He和N2化学性质都很稳定 |
溴化碘(IBr)的化学性质很像卤素的单质,它能与大多数金属、非金属化合生成卤化物,它也能与水发生以下反应:IBr+H2O=HBr+HIO,下列有关IBr的叙述中,不正确的是( )。
| A.在很多反应中IBr是强氧化剂 |
| B.IBr与水反应时既作氧化剂,又作还原剂 |
| C.IBr与AgNO3溶液反应会生成AgBr沉淀 |
| D.IBr与NaOH溶液反应时,生成NaBr和NaIO |
金属元素钫(Fr)在自然界中含量极少。它的21个已知同位素都有放射性。它是碱金属元素中最重的元素。根据它在周期表中的位置预言其性质,其中不正确的是( )。
| A.在已知碱金属元素中具有最大的原子半径 |
| B.在空气中燃烧时生成氧化物Fr2O |
| C.氧化物对应的水化物是极强的碱 |
| D.其单质的熔点比金属钠的熔点低 |