用NaOH溶液吸收二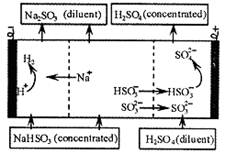
氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴阳膜组合循环再生机理如图,则下列有关说法正确的是( )
| A.阳极区酸性减弱 |
| B.阴极区电极反应式为:2H++2e—=H2↑ |
| C.该过程主要是为了获得H2SO4 |
| D.电解时两个电极都只能用惰性材料 |
下列实验操作中,不合理的是( )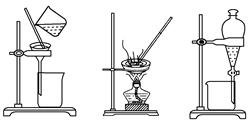
①②③
| A.洗涤沉淀时(如图①),向漏斗中加适量水,搅拌并滤干 |
| B.用CCl4提取碘水中的碘,选③ |
| C.蒸馏时蒸馏烧瓶中液体的体积不能超过容积的2/3,液体也不能蒸干 |
| D.粗盐提纯,选①和② |
如果你家里的食用花生油混有水份,你将采用下列何种方法分离( )
| A.过滤 | B.蒸馏 | C.分液 | D.萃取 |
(6分)请写出下列反应的化学方程式:
(1)实 验 室 制 取 乙 炔 的 化 学 方 程 式 是。
(2)乙醇的催化氧化:。
(3)写出由苯丙烯( 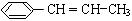 )在催化剂作用下生成聚苯丙烯的反应方程式:
)在催化剂作用下生成聚苯丙烯的反应方程式:
。
由苯、乙醛和乙二醇组成的混和物中,测得含碳元素的质量百分含量为72%,则混和物中氧元素的质量分数为
| A.6% | B.19.6% | C.22% | D.24.9% |
始祖鸟烯(Pterodactyladiene),形状宛如一只展翅飞翔的鸟,其键线式如下图,其中R1、R2为烷烃基。则下列有关始祖鸟烯的说法中正确的是
| A.始祖鸟烯与乙烯互为同系物 |
| B.若Rl=R2=—CH3,则其化学式为C12H16 |
| C.若R1=R2,一定条件下烯烃双键碳原子上的氢也能取代,则始祖鸟烯环上的二氯代物有10种 |
| D.始祖鸟烯既能使酸性高锰酸钾褪色也能使溴水褪色,其褪色原理是一样 |