对反应的方向起作用的因素的判断不正确的是( )
| A.有时焓变对反应的方向起决定作用 |
| B.有时熵变对反应的方向起决定作用 |
| C.焓变和熵变是判断反应的两个主要因素 |
| D.任何情况下,温度都不可能对反应的方向起决定性作用 |
FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,当NO2、N2O4、NO的物质的量之比为1︰1︰1时,实际参加反应的FeS与HNO3的物质的量之比为()
| A.1∶6 | B.1∶7 | C.2∶11 | D.16∶25 |
下列叙述正确的是()
| A.常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在K+、Na+、AlO2-、SO42- |
| B.常温时,0.1mol/L HA溶液的pH>1,0.1mol/L BOH溶液中c(OH-)/c(H+)=1012,将这两种溶液等体积混合,混合后溶液中离子浓度的大小关系为:c(B+)>c(OH-)>c(H+)>c(A-) |
| C.过量SO2通入到Ba(NO3)2溶液中,正确的离子反应方程式为:3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO↑+4H+ |
| D.常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c(NH4+)、c(H+)均下降 |
某澄清透明溶液中只可能含有①Al3+;② Mg2+;③Fe3+;④Fe2+;⑤H+;⑥CO32+;⑦NO3-中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示。则该溶液中一定含有的离子是:()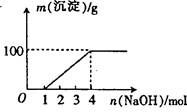
| A.②⑤⑥⑦ | B.②③⑤⑦ |
| C.①②③⑥⑦ | D.①②③④⑤⑦ |
将5.1g镁铝合金,投入到500mL2.0mol/L的盐酸中,金属完全溶解,再加入4.0mol/L的NaOH溶液,若要生成的沉淀最多,则NaOH溶液的体积是:()
| A.200mL | B.250ml | C.425mL | D.560mL |
已知某化学反应A2(g)+2B2(g)=2AB2(g)(AB2的分子结构为B-A-B)的能量变化如图所示,下列有关叙述中正确的是:
A.该反应的进行一定需要加热
B.该反应的ΔH=-(E1-E2)kJ·mol-1
C.该反应中反应物的键能总和大于生成物的键能总和
D.断裂1molA-A键和2molB-B键放出E1kJ能量