下列有关物质的性质和该性质的应用均正确的是 ( )
| A.常温下浓硫酸能使铝发生钝化,则在常温下可用铝制容器储运浓硫酸 |
| B.二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C.MgO和Al2O3在工业上用于制作耐高温材料,也用于电解法冶炼镁、铝金属 |
| D.铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀 |
在一定条件下,密闭容器中可发生可逆反应:N2(g) + 3H2(g)  2NH3(g) 。
2NH3(g) 。
下列说法中,表明这一反应已经达到化学平衡状态的是()
| A.N2、H2、NH3的浓度相等 | B.N2、H2、NH3的浓度不再变化 |
| C.N2、H2、NH3在密闭容器中共存 | D.反应停止,正、逆反应速率都等于零 |
下列各组物质中,互为同分异构体的是()
| A.O2和O3 | B.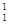 H和 H和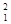 H H |
| C.CH4和CH3CH3 | D.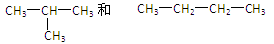 |
下列物质中含有离子键的是()
| A.Br2 | B.CO2 | C.NaBr | D.H2O |
下图所示是短周期的一部分。已知B原子与C原子核外电子总数之和为 A 原子核外电子数的4倍,则以下推断不正确的是( )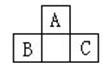
| A.A,B,C三者一定不是非金属元素 |
| B.A,B,C三者核电荷数之和为40 |
| C.A与B,A与C均可形成共价化合物 |
| D.A与B元素存在同素异形现象 |
下列物质的性质比较,正确的是()
| A.酸性:H2SO4>HClO4 | B.碱性:NaOH>KOH |
| C.非金属性: P>S | D.气态氢化物稳定性: HCl>H2S |