下图所示是短周期的一部分。已知B原子与C原子核外电子总数之和为 A 原子核外电子数的4倍,则以下推断不正确的是( )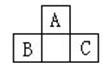
| A.A,B,C三者一定不是非金属元素 |
| B.A,B,C三者核电荷数之和为40 |
| C.A与B,A与C均可形成共价化合物 |
| D.A与B元素存在同素异形现象 |
恒温恒容时,向体积为2.0L密闭容器中充入1.0 molPCl5,反应PCl5(g) PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
| t/s |
0 |
50 |
150 |
250 |
350 |
| n(PCl3)/ mol |
0 |
0.16 |
0.19 |
0.20 |
0.20 |
下列说法正确的是
A.反应在前50 s的平均速率为v(PCl3)="0.0016" mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时,c(PCl3)="0.12" mol·L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20molCl2,达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0mol PCl3、2.0mol Cl2,达到平衡时,PCl3的转化率小于80%
用来表示可逆反应2A(g) + B(g) 2C(g) ;△H<0的正确图像为
2C(g) ;△H<0的正确图像为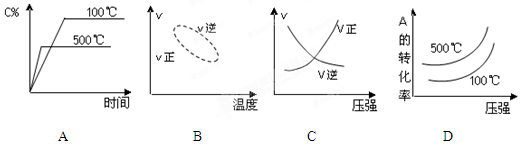
恒温恒容的密闭容器中盛有2mol SO3,发生反应2SO3(g)  2SO2(g)+O2(g),一定条件下平衡时SO2所占的体积百分数为M,若相同条件相同容器中,最初放入4 mol SO3,则平衡时,SO2的体积百分数为N,下列结论正确的是
2SO2(g)+O2(g),一定条件下平衡时SO2所占的体积百分数为M,若相同条件相同容器中,最初放入4 mol SO3,则平衡时,SO2的体积百分数为N,下列结论正确的是
| A.M=N | B.M>N | C.M<N | D.无法比较 |
阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池反应为:2H2+O2=2H2O,电解液为KOH,反应保持在较高温度,使H2O蒸发,下列叙述正确的是
| A.此电池工作时会发出蓝色火焰 |
| B.燃料电池具有能量转化率高、可持续使用的优点 |
| C.该电池的负极电极反应式为:2H2+4e-=4H+; |
| D.该电池的正极电极反应式为:O2+2H2O+4e -=4OH- |
下列有关说法正确的是
A.反应NH3(g)+HCl(g) NH4Cl(s)在室温下可自发进行,则该反应的ΔH<0 NH4Cl(s)在室温下可自发进行,则该反应的ΔH<0 |
| B.稀氨水中加入氢氧化化钠固体少量,由于氨水的电离平衡逆向移动,所以溶液的碱性减弱 |
| C.电解法精炼铜时,以粗铜作阴极,纯铜作阳极 |
D.CH3COOH溶液加水稀释后,溶液中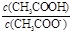 的值减小 的值减小 |