氯化铁溶液与氢氧化铁胶体具有的共同性质是 ( )
| A.分散质颗粒直径都在1nm-100nm之间 | B.能透过半透膜 |
| C.加热蒸干、灼烧后都有氧化铁生成 | D.呈红褐色 |
如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是()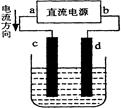
| A.a为负极,b为正极 |
| B.a为阳极,b为阴极 |
| C.电解过程中,d电极质量增加 |
| D.若反应过程中,有2.24 L气体产生,则有0.2 mol电子发生转移 |
关于化学反应热效应的叙述中,正确的是( )
| A.放热反应在常温下就一定很容易发生 | B.放热反应中反应物的总能量大于生成物的总能量 |
| C.化学反应过程中,化学能一定转化成热能 | |
| D.凡是需加热才能进行的反应—定是吸热反应 |
下列化学式既能表示物质的组成,又能表示物质的一个分子的是()
| A.NaOH | B.SiO2 | C.Fe | D.CO2 |
a、b代表2种金属,下列叙述中,肯定能判断金属活动性a比b强的是





 ()
()

A.常温下,a能从水中置换出氢,而b不能 |
B.原子的电子层数a比b多 |
C.原子的最外层电子数a比b少 |
D.1 mol a 、b分别与足量盐酸反应,生成H2的质量a比b大 |
不能用来区别甲烷和乙烯的是()
| A.酸性高锰酸钾溶液 | B.溴水 |
C.溴的四氯化碳溶液 | D.H2 |