下列物质的制备操作,可以达到实验目的是( )
| A.向FeCl3溶液中不断加入NaOH溶液制备Fe(OH)3胶体 |
| B.用铁和Cl2加热制取FeCl3 |
| C.用铜粉和硫粉混合加热制备CuS |
| D.向铝盐溶液中不断滴入烧碱溶液制备Al(OH)3 |
下列说法正确的是( )
| A.SiO2制成的玻璃纤维,由于导电能力强而被用于制造通讯光缆 |
| B.由于Fe可被浓H2SO4氧化,因此常温下不能用钢瓶贮存浓H2SO4 |
| C.镁铝合金的熔点比镁和铝都高 |
| D.不能用氨水鉴别Al3+、Mg2+、Ag+ |
已知碳碳单键可以绕键轴旋转,某烃的结构简式如图,下列说法中正确的是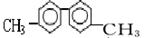
| A.该烃分子的核磁共振氢谱图中有6个吸收峰 |
| B.该烃的一氯代物最多有四种 |
| C.分子中至少有10个碳原子处于同一平面上 |
| D.该烃是苯的同系物,能使高锰酸钾和溴水褪色 |
如图有机物分子中带“*”碳原子是手性碳原子(连有四个不同基团的碳原子)。该有机物分别发生下列反应,生成的有机物分子中不会含有手性碳原子的是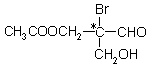
①与甲酸发生酯化反应 ②与足量NaOH水溶液反应
③与银氨溶液作用只发生银镜反应 ④催化剂作用下与H2反应
| A.①②③④ | B.①③ | C.②④ | D.以上反应都不成立 |
某有机物的分子式为C5 H4ClF3,就其结构来说,该有机物不可能是
| A.含两个双键的链状化合物 | B.只含—个双键的链状化合物 |
| C.只含一个三键的链状化合物 | D.只含一个双键的环状化合物 |