某校化学研究性学习小组利用下面所提供的仪器装置和药品制取NaHCO3溶液,设计如下实验。实验室提供的药品、仪器装置如下:
药品:①2% NaOH溶液 ②稀HCl ③稀H2SO4 ④饱和KHCO3溶液 ⑤浓H2SO4 ⑥CaCO3固体 ⑦K2CO3粉末
仪器装置(如图所示):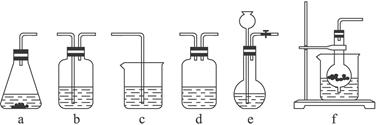
请根据题目要求完成下列问题:
(1)请按下表要求,填写选择的装置和药品。
| 分项 内容 |
CO2发生装置(随开随用,随关随停)(X) |
除杂洗气装置(Y) |
制备产品装置(Z) |
| 选择的装置(填序号) |
|
|
c |
| 选择的药品(填序号) |
|
|
① |
(2)如何检验所选择的CO2发生装置(X)的气密性,请写出主要操作过程:_________________。
(3)将装置按X、Y、Z顺序连接并检查气密性后,当加入药品实验时,X装置中发生化学反应的离子方程式为________________________,Y装置中除去的杂质为_____________。
(4)常温下,向Z装置的NaOH溶液中通入过量CO2气体,其目的是____________________。
(5)若要保证Z装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过_______________%(质量分数)。
附:有关物质在常温(25 ℃)时的溶解度
| 化学式 |
Na2CO3 |
NaHCO3 |
NaOH |
NaCl |
Na2SO4 |
| 溶解度(g/100 g H2O) |
21.3 |
9.60 |
107 |
35.8 |
19.4 |
有A、B、C三块金属浸泡在稀硫酸中,用导线两两相连要以组成各种原电池。若A、B相连,A为负极;B、C相连,B上有气泡逸出;A、C相连,A极减轻。则三种金属的活动性顺序由大到小排列为。
向一个小烧杯中加入20克蔗糖,加3~4滴水,再加入20ml浓硫酸,观察到的实验现象是:烧杯发热、蔗糖变黑、体积膨胀,变成疏松多孔的海棉状的炭,并放出有制激性气味的气体。这个过程表现出浓硫酸的特性是。
下图是教师演示的两个实验(铁架台等辅助仪器略去未画)。回答下列问题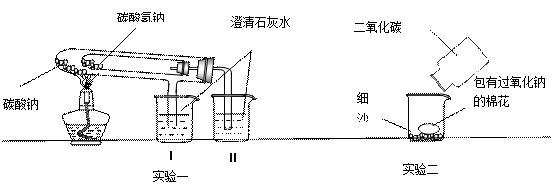
(1)实验一的两烧杯中可以观察到的实验现象是:
I、II、。加热,试管里发生反应的化学方程式是:
(2)实验二用来验证Na2O2与CO2的反应,观察到的实验现象是:含有Na2O2的棉花燃烧。由该实验可以得出许多结论,请写出你所得出的两个结论:
结论1:结论2:
某化学课外活动小组将氯化钠固体中混有的硫酸钠、碳酸氢铵杂质除去并得到氯化钠溶液,设计了如下方案:
|
|
|
某学生设计了以下验证乙二酸(HOOC—COOH)(俗称草酸)的一些性质的实验,根据实验回答下列问题:
(1)用pH值试纸验证乙二酸的酸性,其操作步骤是:。
(2)已知:草酸在175℃时受热分解可生成H2O、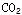 和CO;
和CO;
Ⅰ.该学生设计了下图实验装置,来证明草酸分解产物中有CO并证明其氧化产物。回答有关问题:
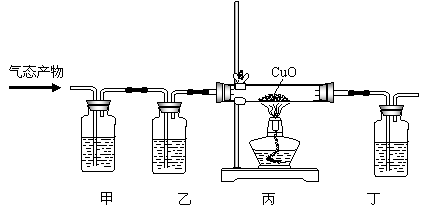 |
①上述实验装置中三个洗气瓶分别盛有澄清石灰水、氢氧化钠溶液、浓硫酸,则甲应盛,乙应盛;
②丙中玻璃管中的现象为:;
③丁装置作用是。
Ⅱ.在实验过程中,该学生发现应对上述实验装置进行一些改进,才能保证实验的科学性和安全性(所选装置如下图)。请回答下列问题: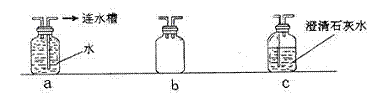
①为确证通往玻璃管的CO气体中已除去CO2,可在甲和乙之间连接。(填上面装置序号)
②在装置丙和丁之间连接b装置,其作用是。
③从环境保护的角度看,应增加尾气处理装置,你如何进行尾气处理,