有A、B、C三块金属浸泡在稀硫酸中,用导线两两相连要以组成各种原电池。若A、B相连,A为负极;B、C相连,B上有气泡逸出;A、C相连,A极减轻。则三种金属的活动性顺序由大到小排列为 。
I、通过火法冶金炼出的铜是粗铜,含杂质金、银、铁、锌等金属和少量矿物杂质(与酸不反应)。制作电器及其他仪器产品时必须要求是纯铜,为此以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯。
表:几种物质形成沉淀时的pH
| 物质 |
Fe(OH)2 |
Fe(OH)3 |
Zn(OH)2 |
Cu(OH)2 |
| 开始沉淀时的pH |
7.6 |
2.7 |
5.7 |
4.7 |
| 完全沉淀时的pH |
9.7 |
3.7 |
8.5 |
7.3 |
(1)在精炼铜时,阴极电极反应方程式为 ;金、银以单质的形式沉积在电解槽 (填“阳极”或“阴极”)的槽底。
(2)在精炼铜的过程中,Cu2+浓度逐渐降低,c(Fe2+)、c(Zn2+)会逐渐增大,所以需定时除去其中的Fe2+、Zn2+。甲同学设计了如下除杂流程:
|
①试剂a最好选用 (填写序号),加入试剂a的目的是 。
a、氯水 b、高锰酸钾溶液 c、硝酸 d、双氧水| 难溶电解质 |
AgI |
AgOH |
Ag2S |
PbI2 |
Pb(OH)2 |
PbS |
| Ksp |
8.3×10-17 |
5.6×10-8 |
6.3×10-50 |
7.1×10-9 |
1.2×10-15 |
3.4×10-28 |
(1)你认为往废水中投入 (填字母序号)沉淀的效果最好
a、NaOH b、Na2S c、KI d、Ca(OH)2
(2)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=
原电池是化学对人类的一项重大贡献。
(1)某兴趣小组为研究原电池原理,设计如图装置。
①a和b不连接时,烧杯中发生反应的离子方程式是__________。
②a和b用导线连接,Cu极为原电池__________极(填“正”或“负”),电极反应式是__________。Zn极发生__________(填“氧化”或“还原”)反应。溶液中H+移向__________(填“Cu”或“Zn”)极。
③无论a和b是否连接,Zn片均被腐蚀。若转移了0.2mol电子,则理论上Zn片质量减轻了__________g。
(2)有同学想把Ba(OH)2•8H2O晶体与NH4Cl晶体的反应设计成原电池,你认为是否可行?________(填“是”或“否”),理由是__________。
某同学进行如下实验:
向盛有10滴 溶液的试管中滴加
溶液的试管中滴加 溶液,至不再有白色沉淀生成。向其中滴加
溶液,至不再有白色沉淀生成。向其中滴加 溶液;再向其中滴加
溶液;再向其中滴加 的
的 溶液。
溶液。
请回答:
(1)白色沉淀是,证明“不再有白色沉淀生成”的操作是。
(2)能说明 溶解度依次减小的现象为。
溶解度依次减小的现象为。
(3)滴加 溶液后发生反应的离子方程式是。
溶液后发生反应的离子方程式是。
某化学小组设计实验验证温度对化学反应速率的影响。
【实验用品】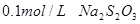 溶液、
溶液、 、烧杯、冷水、热水、秒表等
、烧杯、冷水、热水、秒表等
【实验步骤】
I.取两支试管各加入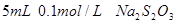 。
。
II. 另取两支试管各加入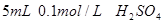 。
。
III. ……
IV. 一段时间后,分别混合并搅拌。
V. 记录实验现象及数据。
(1)步骤III的操作为。
(2)该实验需要记录的实验数据是。
(3)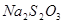 和
和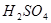 反应的化学方程式为。
反应的化学方程式为。
(4)能说明温度升高反应速率增大的现象是。
实验室里常见到右图所示仪器,该仪器为两头密封的玻璃管,中间带有一根玻璃短柄。该仪器可进行多项实验。当玻璃管内装有碘晶体时,用此仪器可进行碘升华实验,具有装置简单、操作方便、现象明显、没有污染,可反复使用等优点。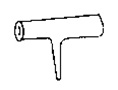
(1)用此仪器不能反复进行的实验是(填序号)
| A.NH4Cl固体受热分解 | B.KMnO4晶体受热分解 |
| C.白磷和红磷一定温度下互相转变 | D.无水CuSO4和胆矾的互变实验 |
(2)当玻璃管内装有NO2和N2O4的混合气体时,亦可反复进行反应条件对化学平衡影响的实验,该实验的操作过程和实验现象是
_____________________________________________________________。
(3)如果玻璃管内装有大量红色溶液,加热时溶液颜色变浅,冷却时恢复红色,该溶液可能是,如果玻璃管内封有少量无色溶液,加热溶液时,溶液变红,冷却后恢复无色。此溶液可能是。